题目内容
【题目】某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其中不合理的是
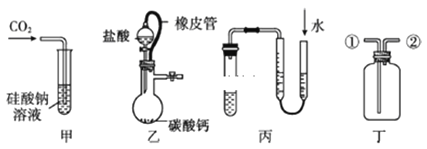
A. 甲装置:可用来证明碳酸的酸性比硅酸强
B. 乙装置:橡皮管的作用是平衡气压,使液体顺利流下
C. 丙装置:用图示的方法不能检查此装置的气密性
D. 丁装置:先从①口进气集满二氧化碳,再从②口进气,可收集氢气
【答案】C
【解析】
碳酸的酸性大于硅酸,根据强酸制取弱酸判断;橡皮管的作用是能让分液漏斗和蒸馏烧瓶间压强平衡;利用压强差检验装置的气密性;根据气体的溶解性及密度确定收集方法。
二氧化碳和水反应生成碳酸,碳酸酸性大于硅酸,所以二氧化碳和硅酸钠溶液反应生成不溶性硅酸,则该装置能证明碳的非金属性比硅强,A正确;分液漏斗和蒸馏烧瓶间用橡皮管连接,可使它们之间气体流通,保证了分液漏斗和蒸馏烧瓶间压强平衡,能使水顺利流下,B正确;如果装置的气密性良好,甲、乙两侧水面高度不同,否则水面相同,所以能检验装置的气密性,C错误;二氧化碳的密度大于空气、氢气的密度小于空气,所以氢气采用向下排空气法收集、二氧化碳采用向上排空气法收集,D正确。
故选C。

【题目】
(1)根据计算用托盘天平需称取氯化钠_________ g;
(2)配制溶液时,除需要烧杯、玻璃棒外,还必须用到的玻璃仪器有 ;
(3)配制溶液有下列几步操作:a.溶解,b.摇匀,c.洗涤,d.冷却,e.称量,f.将溶液移至容量瓶,g.定容.正确的操作顺序是 ;
(4)下列操作结果使溶液物质的量浓度偏低的是___ ______ ;
A.没有将洗涤液转入容量瓶中 |
B.加水定容时,水的量超过了刻度线 |
C.定容时,俯视容量瓶的刻度线 |
D.容量瓶洗涤后,未经干燥处理 |
(5)取出该NaCl溶液10mL加水稀释到200mL,稀释后溶液中NaCl的物质的量浓度是_________