题目内容
【题目】化学反应中的能量变化是由化学反应中旧化学健断裂时吸收的能量与化学健形成时放出的能量不同引起的。如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法中正确的是
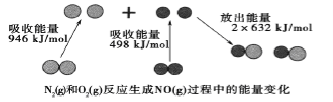
A.1molN2(g)和1molO2(g)反应放出的能量为180kJ
B.1molN2(g)和1molO2(g)具有的总能量小于2molNO(g)具有的总能量
C.在1L的容器中发生反应.10min内N2减少了1mol,因此10min内的平均反应速率为v(NO)=0.1mol/(L·min)
D.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
【答案】B
【解析】
试题分析:A.反应热就是断键吸收的能量和形成化学键所放出的能量的差值,所以该反应的反应热是946kJ/mol+498kJ/mol-2×632kJ/mol=+180kJ/mol,所以该反应是吸热反应,A项错误,B.根据上述分析,该反应为吸热反应,1molN2(g)和1molO2(g)具有的总能量小于2molNO(g)具有的总能量,B项正确;C.10min内N2减少了1mol,则NO增加了2moL,因此10min内的平均反应速率为v(NO) = 2mol ÷ (1L × 10min)=0.2mol/(L·min),C项错误;D.NO与NaOH不反应,不是酸性氧化物,D项错误;答案选B。

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目