题目内容
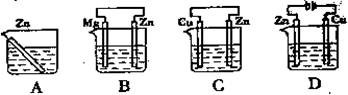
某同学按图示装置进行实验:A极是铜锌合金,B极为纯铜,溶液为足量的硫酸铜溶液。通电一段时间后,若A极恰好全部溶解,此时B极质量增加5.76g,溶液质量增0.03g,则合金中Cu、Zn原子个数比为
| A.4:1 | B.3:1 | C.2:1 | D.任意比 |
C
解析试题分析:阳极A极是铜锌合金,发生反应:Zn-2e-=Zn2+;Cu-2e-=Cu2+.阴极B极为纯铜,发生反应Cu2+ +2e-= Cu。n(Cu)= 5.76g÷64g/mol=0.09mol.由于Zn、Cu都是+2价的金属,所以阳极溶解的合金的物质的量也是0.09mol。1摩尔的Zn质量是65g,1摩尔的Cu质量是64g,相差1g. 现在溶液质量增0.03g,说明合金中含有Zn的物质的量为n(Zn)=0.03mol,n(Cu)=0.06mol.因此n(Cu): n(Zn)=0.06:0.03=2:1.即二者的个数比为2:1.选项为C。
考点:考查电解池、金属的精炼的知识

练习册系列答案
相关题目
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是
A.用惰性电极电解饱和食盐水时,阳极的电极反应式为:2Cl- – 2e-=Cl2 |
| B.氢氧燃料电池的负极反应式:O2 + 2H2O + 4e-= 4OH- |
| C.粗铜精炼时,与电源正极相连的是纯铜,电极反应为:Cu – 2e-= Cu2+ |
| D.钢铁发生电化学腐蚀的正极反应式:Fe – 2e- = Fe2+ |
下列叙述正确的是
| A.纯锌与硫酸反应时,加入少量CuSO4溶液,可使反应速率加快 |
| B.甲醇和氧气以及KOH溶液构成的新型燃料电池中,其负极上发生的反应为:CH3OH+6OH- +6e-=CO2 +5H2O |
| C.在铁件上镀铜时,金属铜作阴极 |
| D.电解精炼铜时电解质溶液中铜离子浓度保持不变 |
将等物质的量浓度的CuSO4溶液和NaCl溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图,则下列说法正确的是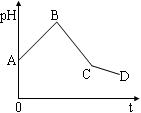
| A.阳极产物一定是Cl2,阴极产物一定是Cu |
| B.BC段表示在阴极上是H+放电产生了H2 |
| C.整个过程中阳极先产生Cl2,后产生O2 |
| D.CD段表示阳极上OH-放电破坏了水的电离平衡,产生了H+,故pH减小 |
下列有关金属腐蚀与防护的说法正确的是
| A.纯银器表面在空气中会因化学腐蚀渐渐变暗 |
| B.地下输油钢管与外加直流电源的正极相连可保护其不受腐蚀 |
| C.海轮外壳连接锌块是采用牺牲阴极的阳极保护法保护外壳不受腐蚀 |
| D.当镀锡铁制品的镀层破损时,锡镀层仍能对铁制品起保护作用 |
某位同学利用家中废旧材料制作了一个可使玩具扬声器发出声音的装置,如图。下列有关该电池工作时的说法错误的是( )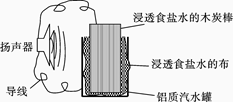
| A.铝罐将逐渐被腐蚀 |
| B.电子流向为铝质汽水罐→导线→扬声器→导线→炭棒 |
| C.食盐水中的Na+向炭棒移动 |
| D.炭棒上发生的反应为:2H++2e-=H2↑ |
人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.下图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是
| A.该过程是将太阳能转化为化学能的过程 |
| B.催化剂a表面发生氧化反应,有O2产生 |
| C.催化剂a附近酸性减弱,催化剂b附近酸性增强 |
| D.催化剂b表面的反应是CO2+2H++2e-====HCOOH |
在钢铁的电化腐蚀中,正极上发生的反应可能是
| A.Fe - 2e—=Fe2+ | B.O2+4e-+2H2O=4OH- |
| C.4OH- - 4e-=O2↑+2H2O | D.4Fe(OH)2+O2+2H2O =4Fe(OH)3 |