题目内容
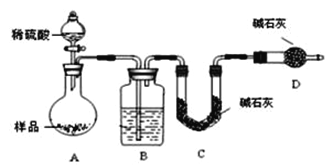
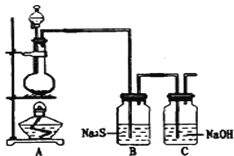
【题目】某学生为了验证苯酚、醋酸和碳酸的酸性强弱,设计了如图所示实验装置。

请回答下列问题:
(1)仪器B中的实验现象:____________________________________________。
(2)仪器B中发生反应的化学方程式是___________________________。
(3)该实验设计不严密,请改正:____________________________________________________________。
【答案】 溶液由澄清变浑浊 C6H5ONa+H2O+CO2![]() C6H5OH+NaHCO3 在A、B之间连接一个洗气瓶,洗气瓶内盛饱和碳酸氢钠溶液,吸收挥发出来的醋酸
C6H5OH+NaHCO3 在A、B之间连接一个洗气瓶,洗气瓶内盛饱和碳酸氢钠溶液,吸收挥发出来的醋酸
【解析】试题分析:(1)醋酸与石灰石反应生成CO2,碳酸的酸性强于苯酚的。因此CO2通入到苯酚钠溶液中会生成苯酚,所以仪器B中的实验现象是溶液由澄清变浑浊。
(2)由于碳酸的酸性强于苯酚的,而苯酚的酸性又强于碳酸氢纳的,所以CO2与苯酚钠反应生成苯酚和碳酸氢纳,则仪器B中反应的化学方程式为C6H5ONa+H2O+CO2→ C6H5OH+NaHCO3。
(3)因为醋酸易挥发,所以生成的CO2气体中含有醋酸,醋酸也能和苯酚钠反应生成苯酚,因此实验设计不严密。要改正只需要在A、B之间连接洗气装置,洗气液为饱和NaHCO3溶液,吸收挥发的醋酸即可。

练习册系列答案
相关题目