题目内容
下图是一个乙醇燃料电池常温工作原理示意图,乙池中的两个电极一个

是石墨电极,一个是铁电极。工作时M、N两个电极的质量都不减少,则下列说法正确的是

是石墨电极,一个是铁电极。工作时M、N两个电极的质量都不减少,则下列说法正确的是
| A.M电极的材料是石墨 |
| B.若乙池中某一电极质量增加4.32g时,理论上消耗氧气为448ml |
| C.在此过程中,甲池中OH-向通乙醇的一极移动 |
| D.在此过程中,乙池溶液中电子从M电极向N电极移动 |
C
通入乙醇的电极为原电池的负极,M 为电解池的阴极,通入氧气的电极为原电池的正极,N 为电解池的阳极,工作时M、N两个电极的质量都不减少,所以阳极为惰性电极,N电极的材料是石墨,M电极的材料为铁,A 错误。
若乙池中某一电极质量增加4.32g时,增加的是银的质量,4.32/108=0.04,得到0.04mol银,转移0.04mol电子,上消耗氧气为224ml,B 错误
甲池为原电池,阴离子向负极移动,OH-向通乙醇的一极移动,C 正确。
乙池溶液中电子从N电极向M电极移动
若乙池中某一电极质量增加4.32g时,增加的是银的质量,4.32/108=0.04,得到0.04mol银,转移0.04mol电子,上消耗氧气为224ml,B 错误
甲池为原电池,阴离子向负极移动,OH-向通乙醇的一极移动,C 正确。
乙池溶液中电子从N电极向M电极移动

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
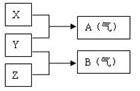
 2Ag + Zn(OH)2,下列说法正确的是
2Ag + Zn(OH)2,下列说法正确的是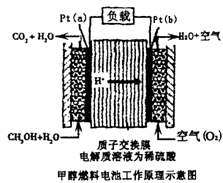
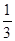 mol
mol
 Na2Sx,以下说法错误的是
Na2Sx,以下说法错误的是