题目内容
设NA表示阿伏加德罗常数的值,下列说法不正确的是
| A.15 g C2H6含C—H键数目为3NA |
| B.28 g乙烯与丙烯的混合气体,含碳原子总数为2NA |
| C.标准状况下,11.2 L O2与足量Na加热反应,转移电子总数为NA |
| D.铜与浓H2SO4反应,当转移电子数为NA时,收集SO2体积为11.2 L |
D
解析试题分析:A、15 g C2H6的物质的量是0.5mol,含C—H键数目为3NA,正确;B、乙烯与丙烯的混合气体的最简式为CH2,所以28 g乙烯与丙烯的混合气体,含碳原子总数为2NA,正确;C、标准状况下,11.2 L O2的物质的量是0.5mol,转移电子的物质的量是0.5mol×2=1mol,正确;D、未指明标准状况,所得气体的体积无法确定,错误,答案选D。
考点:考查阿伏伽德罗常数对理解应用

练习册系列答案
相关题目
下列说法正确的是(NA表示阿伏加德罗常数的值)
| A.1 mol聚乙烯含有的原子数目为6NA |
| B.标准状况下,11.2L CHCl3中所含有的原子总数为2.5NA |
| C.一定条件下,2.6 g乙炔、苯和苯乙烯的气态混合物中所含碳原子数为0.2NA |
| D.1 mol甲基含10 NA个电子 |
下表为四种溶液的溶质质量分数和物质的量浓度的数值,根据表中数据判断四种溶液中密度最小的是
| 溶液 | KOH | HNO3 | CH3COOH | HCl |
| 溶质质量分数w(%) | 56 | 63 | 60 | 36.5 |
| 物质的量浓度c(mol·L-1) | 14.3 | 13.8 | 10.6 | 11.8 |
A.HCl B.HNO3 C.CH3COOH D.KOH
设NA表示阿伏加德罗常数的数值,下列说法正确的是( )。
| A.25 ℃时,pH=2的1.0 L H2SO4溶液中含有H+的数目为0.02 NA |
B.0.5 mol雄黄(As4S4,所有原子都满足8电子结构,结构如图)含有NA个S—S键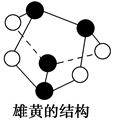 |
| C.39 g苯分子中共含6 NA个共价单键 |
| D.向FeI2、NaBr的混合溶液中通入适量氯气,当有1 mol Fe2+被氧化时,该反应转移电子的数目至少为3 NA |
在下列条件下,两种气体的分子数一定相等的是 ( )。
| A.同密度、同压强的N2和C2H4 |
| B.同温度、同体积的O2和N2 |
| C.同体积、同密度的C2H4和CO |
| D.同压强、同体积的O2和N2 |
在标准状况下,用干燥烧瓶收集一瓶氯化氢气体倒置于盛水的水槽中时,水充满烧瓶(假设烧瓶里溶液不扩散出水槽),烧瓶里盐酸的密度为ρ g·cm-3。该盐酸的物质的量浓度、溶质的质量分数分别为( )。
A.c=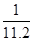 mol·L-1、w= mol·L-1、w=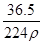 % % |
B.c=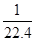 mol·L-1、w= mol·L-1、w=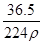 % % |
C.c=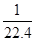 mol·L-1、w= mol·L-1、w=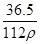 % % |
D.c=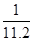 mol·L-1、w= mol·L-1、w=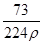 % % |
下列化学用语使用正确的是( )
| A.葡萄糖、淀粉的最简式都是CH2O |
B.CH4的电子式是 |
| C.乙醛分子的结构简式是CH3COH |
D.丙烷分子的球棍模型是 |
某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种物质组成。进行如下实验: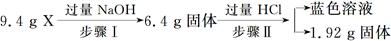
下列有关说法正确的是( )
| A.步骤Ⅰ中减少的3 g固体一定是混合物 |
| B.步骤Ⅱ中质量减少的物质一定是Cu |
| C.根据步骤Ⅰ、Ⅱ可以判断混合物X的成分为Al2O3、Fe2O3、Cu、SiO2 |
| D.根据上述步骤Ⅱ可以得出m(Fe2O3)∶m(Cu)=1∶1 |
