题目内容
以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。
(1)电解饱和食盐水的化学方程式为 。
。
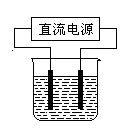
(2)常温下,某化学兴趣小组在实验室中,用石墨电极以右图装置进行电解某浓度氯化钠溶液的实验,电解一段时间后,收集到标准状况下氢气2.24 L。(设电解前后溶液的体积均为1 L,不考虑水的消耗或气体的溶解)
①理论上,电解后溶液中c(OH—)= mol/L。
②若实际测得反应后溶液的c(OH—)=0.1mol/L,则造成这种误差的原因可能是:
a.2H2O 2H2↑+O2↑;若仅考虑该原因,则电解过程中溶液减小的质量是 g。
2H2↑+O2↑;若仅考虑该原因,则电解过程中溶液减小的质量是 g。
b.还可能为 (用离子方程式表示)。
经测定,该实验中溶液实际减少的质量为4.23 g,则所产生的气体及其物质的量之比为 。
(1)电解饱和食盐水的化学方程式为
 。
。(2)常温下,某化学兴趣小组在实验室中,用石墨电极以右图装置进行电解某浓度氯化钠溶液的实验,电解一段时间后,收集到标准状况下氢气2.24 L。(设电解前后溶液的体积均为1 L,不考虑水的消耗或气体的溶解)

①理论上,电解后溶液中c(OH—)= mol/L。
②若实际测得反应后溶液的c(OH—)=0.1mol/L,则造成这种误差的原因可能是:
a.2H2O
 2H2↑+O2↑;若仅考虑该原因,则电解过程中溶液减小的质量是 g。
2H2↑+O2↑;若仅考虑该原因,则电解过程中溶液减小的质量是 g。b.还可能为 (用离子方程式表示)。
经测定,该实验中溶液实际减少的质量为4.23 g,则所产生的气体及其物质的量之比为 。
(1)2NaCl+2H2O H2↑+Cl2↑+2NaOH (3分)
H2↑+Cl2↑+2NaOH (3分)
(2)①0.2 (3分) ②4.55 (2分) Cl2+2OH —=Cl—+ClO—+H2O(2分)
—=Cl—+ClO—+H2O(2分)
n(H2)∶n(Cl2)∶n(O2)=20∶10∶3 (2分)
 H2↑+Cl2↑+2NaOH (3分)
H2↑+Cl2↑+2NaOH (3分) (2)①0.2 (3分) ②4.55 (2分) Cl2+2OH
 —=Cl—+ClO—+H2O(2分)
—=Cl—+ClO—+H2O(2分) n(H2)∶n(Cl2)∶n(O2)=20∶10∶3 (2分)
略

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

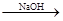 Mg(OH)2
Mg(OH)2 Mg
Mg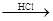 MgCl2溶液
MgCl2溶液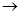 MgCl2熔融
MgCl2熔融 Mg(OH)2
Mg(OH)2 MgO
MgO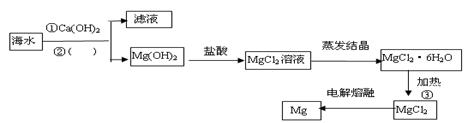
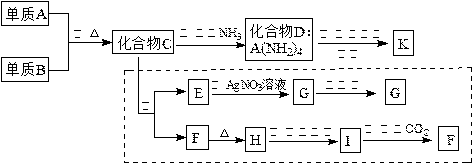
 研究的一项重要任务。
研究的一项重要任务。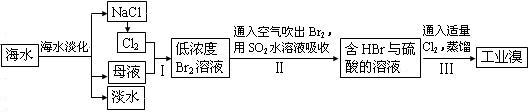
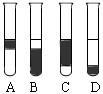 ②在3mL溴水中,加入1mL四氯化碳,振荡、静置后,观察到试管里的分层现象为右图中 ▲ 。
②在3mL溴水中,加入1mL四氯化碳,振荡、静置后,观察到试管里的分层现象为右图中 ▲ 。
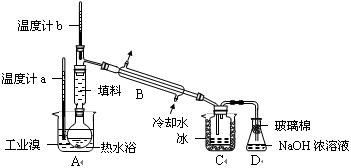
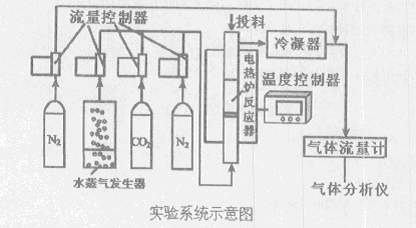
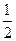 O2(g)=CO2(g) △H=-283kJ/mol
O2(g)=CO2(g) △H=-283kJ/mol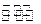 H2(g)+CO2(g)
H2(g)+CO2(g)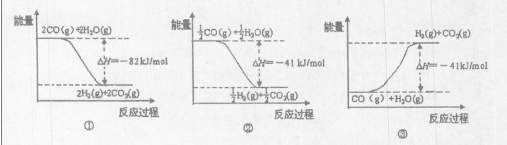
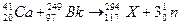 ,该变化不属于化学变化
,该变化不属于化学变化 ),该分子中所有原子可以处于同一平面
),该分子中所有原子可以处于同一平面