题目内容
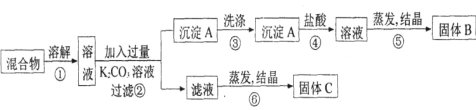
【题目】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物。试回答下列问题:
(1) B物质的化学式为 。
(2) 该方案的明显失误是因某一步设计不当而使分离产物不纯,该步骤是 (填序号)如何改进 ,所涉及反应的离子方程式为 。
(3)写出 ② ④ 两步中对应的离子方程式:
② ;
④____________________________________。
【答案】(1)BaCl2(2)步骤⑥应先在滤液中加过量盐酸,然后再蒸发结晶得固体C
(3)Ba2++CO32-=BaCO3↓;BaCO3+2H+=Ba2++CO2+H2O
【解析】
试题分析:(1)要分离KCl和BaCl2两种固体混合物,加入过量的K2CO3溶液使BaCl2完全转化成BaCO3沉淀。将沉淀洗涤与盐酸反应后经蒸发干燥得到固体B为BaCl2。
(2)加入过量K2CO3溶液后所得的滤液中有KCl和K2CO3,直接加热蒸发结晶所得的固体C(氯化钾)中混有K2CO3,因此步骤⑥应先在滤液中加过量的盐酸与K2CO3反应转化为KCl后,再蒸发结晶得到纯净的KCl。
(3)根据以上分析可知反应②的离子方程式为Ba2++CO32-=BaCO3↓,反应④的离子方程式为BaCO3+2H+=Ba2++CO2+H2O。

练习册系列答案
相关题目