题目内容
【题目】研究表明N2O与CO在Fe+作用下发生反应的能量变化及反应历程如图所示,下列说法错误的是

A. 总反应是放热反应
B. Fe+使反应的活化能降低
C. FeO+也是该反应的催化剂
D. Fe++N2O→FeO++N2、FeO++CO→Fe++CO2两步反应均为放热反应
【答案】C
【解析】
A.由图可知,反应物总能量大于生成物总能量;
B.Fe+作催化剂;
C. FeO+是反应过程的中间产物;
D.由图可知,Fe++N2O→FeO++N2、FeO++CO→Fe++CO2两步中均为反应物总能量大于生成物总能量。
A.由图可知,反应物总能量大于生成物总能量,为放热反应,A正确;
B.Fe+在反应前后的质量和性质保持不变,故其作催化剂,使反应的活化能减小,B正确;
C.催化剂是加入的物质,可以改变反应速率,但其质量和化学性质不变,而FeO+是反应过程的中间产物,因此不是催化剂,C错误;
D.由图可知,Fe++N2O→FeO++N2、FeO++CO→Fe++CO2两步中均为反应物总能量大于生成物总能量,因此二者均为放热反应,D正确;
故合理选项是C。

 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案【题目】短周期五种元素A、B、C、D、E的原子序数依次增大。A、B、C的单质在常温下都呈气态,C原子最外层电子数是电子层数的3倍,C和E位于同主族。1molDAx与足量的A2C反应生成44.8L(标准状况)G气体。A、B的单质依次为G、T,在密闭容器中充入一定量的G、T,一定条件下发生反应G+T→W(未配平),测得各物质的浓度如表所示。
物质 | T | G | W |
10min时,c/(mol/L) | 0.5 | 0.8 | 0.2 |
20min时,c/(mol/L) | 0.3 | 0.2 | 0.6 |
回答下列问题:
(1)A、B、C能组成既含离子键又含共价键的化合物,该化合物的化学式为_________。
(2)B、C、D、E的简单离子中,离子半径由大到小排序为__________。(用离子符号表示)
(3)J、L是由A、B、C、E四种元素组成的两种常见酸式盐,J、L混合可产生有刺激性气味的气体,写出这两种溶液发生反应的离子方程式_______;J、L中能使酸性高锰酸钾溶液退色的是_______(填化学式)。
(4)B2A4-C2碱性燃料电池放电效率高。该电池放电时生成B2和A2C,正极反应式为_____;电池工作一段时间后,电解质溶液的pH_____(填“增大”“减小”或“不变”)。
(5)由A、B、C、D四种元素组成的单质、化合物在一定条件下的转化关系(部分条件和产物已省略)如图所示,已知M耐高温。
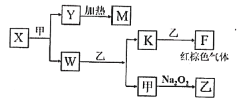
①X的电子式为______;W的结构式为________。
②已知W与乙反应生成K和甲是某重要化工生产步骤之一,提高其反应速率的方法除增大反应物浓度、增大压强外,还有______、______。