��Ŀ����
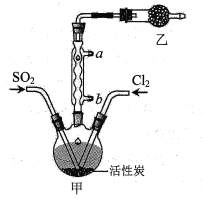
����Ŀ�������ȣ�SO2Cl2���������л��ϳɺ�ҩ������ȡ�ʵ��������SO2��Cl2�ڻ���̿��������ȡSO2Cl2[SO2(g)+Cl2(g)![]() SO2Cl2(l) ��H=-97.3kJ/mol]��װ����ͼ��ʾ������װ��ʡ�ԣ�����֪SO2Cl2���۵�Ϊ��54.1�棬�е�Ϊ69.1�棬��ǿ��ʴ�ԣ����˽Ӵ��������ά�ص�����������л����ˮ�ܷ������ҷ�Ӧ�������������ش��������⣺
SO2Cl2(l) ��H=-97.3kJ/mol]��װ����ͼ��ʾ������װ��ʡ�ԣ�����֪SO2Cl2���۵�Ϊ��54.1�棬�е�Ϊ69.1�棬��ǿ��ʴ�ԣ����˽Ӵ��������ά�ص�����������л����ˮ�ܷ������ҷ�Ӧ�������������ش��������⣺
I��SO2Cl2���Ʊ�
��1��ˮӦ��___��ѡ�a����b�����ڽ��롣
��2����ȡSO2����������___�����ţ���
��Fe+18.4mol/LH2SO4
��Na2SO3+70%H2SO4
��Na2SO3+3mo/LHNO3
��3����װ����ʢ�ŵ��Լ���___��
��4���Ʊ���������Ҫ��װ�ü����ڱ�ˮԡ�У�ԭ����___��
��5����Ӧ����������л��������ʵ�������___��
II���ⶨ��Ʒ��SO2Cl2�ĺ�����ʵ�鲽�����£�
��ȡ1.5g��Ʒ��������Ba(OH)2��Һ����������ˡ�ϴ�ӣ���������Һ��������ƿ�У�
������ƿ�м��������ữ���ټ���0.2000mol��L��1��AgNO3��Һl00.00mL��
�������м���2mL������������ҡ����ʹ�������汻�л��︲�ǣ�
�ܼ���NH4Fe(SO4)2ָʾ������0.1000mol��L-1NH4SCN��Һ�ζ�����Ag+���յ��������Ϊ10.00mL��
��֪��Ksp(AgCl)=3.2��10-10Ksp(AgSCN)=2��10-12
��6���ζ��յ������Ϊ___��
��7����Ʒ��SO2Cl2����������Ϊ___%��������۲�����������������SO2Cl2������___���ƫ�ߡ�����ƫ�͡�����Ӱ�족����
���𰸡�b �� ��ʯ�� ��ȡ�����ȵķ�Ӧʱ���ȷ�Ӧ�������¶�ʹƽ�������ƶ������������SO2Cl2���� ���� ��Һ��Ϊ��ɫ�����Ұ�����ڲ���ɫ 85.5% ƫС
��������
��1��������ȴ��ˮӦ�ô��¿��룬�Ͽڳ���
��2���Ʊ�SO2������Ũ���ᷴӦ��Ҫ���ȣ�����������SO2��������70% H2SO4+Na2SO3���Ʊ�SO2��
��3�������ܵ�������������������Ӧ��û�м��ȣ���SO2��������ķ�ӦΪ���ȷ�Ӧ�����ڻ���һ����Cl2��SO2ͨ���������ݳ���������Ӧʹ�ü����Լ�������SO2Cl2��ˮ��ˮ�⣬���ü�ʯ�ң�
��4����ȡ�����ȵķ�Ӧʱ���ȷ�Ӧ�������¶�ʹƽ�������ƶ������������SO2Cl2���ʣ�
��5������е㲻ͬ��Һ�����������ķ��������Լ��л������뿪��ʵ�����������
��6����0.1000mol��L-1NH4SCN��Һ�ζ�����Ag+���յ㣬���ζ��ﵽ�յ�ʱNH4SCN��������NH4Fe(SO4)2��ָʾ����Fe3+��SCN��Ӧ��Һ����ɫ��������ڲ���ɫ������ȷ���ζ��յ㣻
��7����cmol��L-1NH4SCN��Һ�ζ�����Ag+���յ㣬�����������V�������Ag+�����ʵ���ΪVcmol����Cl��Ӧ��Ag+�����ʵ���Ϊ0.1000mol/L��0.1LVc��103mol����������SO2Cl2�����ʵ����� AgSCN�������ܽ�ȱ�AgClС���ɼ�������������ҡ����ʹAgCl�������汻�л��︲�ǣ������ڵμ�NH4SCNʱ����AgCl����ת��ΪAgSCN���������˲�����NH4SCN��AgCl��Ӧ����AgSCN��������ζ�ʱ���ĵ�NH4SCN��Һ�����ƫ�࣬�������ӵ����ʵ���ƫ�����������ӷ�Ӧ�������ӵ����ʵ���ƫС��
��1��������ȴ��ˮӦ�ô��¿��룬�Ͽڳ�����ˮӦ�ô�b�ڽ��룻
��2���Ʊ�SO2������Ũ���ᷴӦ��Ҫ���ȣ�����������SO2�������â�70% H2SO4+Na2SO3���Ʊ�SO2����ѡ�ڣ�
��3������װ��ͼ��֪�������ܵ�������������������Ӧ��û�м��ȣ���SO2��������ķ�ӦΪ���ȷ�Ӧ�����ڻ���һ����Cl2��SO2ͨ���������ݳ���������Ӧʹ�ü����Լ�������SO2Cl2��ˮ��ˮ�⣬���ü�ʯ�ң���������������SO2����ֹ�����е�ˮ���������������У�����װ����ʢ�ŵ��Լ��Ǽ�ʯ�ң�
��4����ȡ�����ȵķ�Ӧʱ���ȷ�Ӧ�������¶�ʹƽ�������ƶ������������SO2Cl2���ʣ�
��5������е㲻ͬ��Һ�����������ķ��������Լ��л������뿪��ʵ�����������
��6����0.1000mol��L-1NH4SCN��Һ�ζ�����Ag+���յ㣬���ζ��ﵽ�յ�ʱNH4SCN��������NH4Fe(SO4)2��ָʾ����Fe3+��SCN��Ӧ��Һ����ɫ��������ڲ���ɫ������ȷ���ζ��յ㣻�ʴ�Ϊ����Һ��Ϊ��ɫ�����Ұ�����ڲ���ɫ��
��7����0.1000mol��L-1NH4SCN��Һ�ζ�����Ag+���յ㣬�����������10.00mL�������Ag+�����ʵ���ΪVcmol=0.01��0.1000mol��L-1=1��10-3mol����Cl��Ӧ��Ag+�����ʵ���Ϊ0.2000mol/L��0. 1LVc��103mol��1.9��10-2mol����SO2Cl2�����ʵ���Ϊ1.9��10-2mol ��0.5=9.5��10-3mol ����Ʒ��SO2Cl2����������Ϊ![]() ��100%=85.5%�� ��֪��Ksp(AgCl)=3.2��1010��Ksp(AgSCN)=2��1012����AgSCN�������ܽ�ȱ�AgClС���ɼ�������������ҡ����ʹAgCl�������汻�л��︲�ǣ������ڵμ�NH4SCNʱ����AgCl����ת��ΪAgSCN���������˲�����NH4SCN��AgCl��Ӧ����AgSCN��������ζ�ʱ���ĵ�NH4SCN��Һ�����ƫ�࣬�������ӵ����ʵ���ƫ�����������ӷ�Ӧ�������ӵ����ʵ���ƫС�����Բ�õ������ӵ����ʵ���ƫС���ʴ�Ϊ��85.5%��ƫС��
��100%=85.5%�� ��֪��Ksp(AgCl)=3.2��1010��Ksp(AgSCN)=2��1012����AgSCN�������ܽ�ȱ�AgClС���ɼ�������������ҡ����ʹAgCl�������汻�л��︲�ǣ������ڵμ�NH4SCNʱ����AgCl����ת��ΪAgSCN���������˲�����NH4SCN��AgCl��Ӧ����AgSCN��������ζ�ʱ���ĵ�NH4SCN��Һ�����ƫ�࣬�������ӵ����ʵ���ƫ�����������ӷ�Ӧ�������ӵ����ʵ���ƫС�����Բ�õ������ӵ����ʵ���ƫС���ʴ�Ϊ��85.5%��ƫС��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�