题目内容
【题目】设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
A.标准状况下,22.4L己烷含有的共价键总数为19NA
B.1L 0.1 mol·L-1 Na2CO3溶液中阴阳离子数之和为0.3NA
C.16g O2和14C2H4的混合物中所含中子数为8NA
D.密闭容器中l.5mol H2与0.5mol N2充分反应,得到NH3的分子数为NA
【答案】C
【解析】
A、标准状况下,己烷不是气体,22.4L己烷含有的共价键总数大于19NA,故A错误;
B、Na2CO3溶液中存在CO32-+H2O![]() HCO3-+OH-、HCO3-+H2O
HCO3-+OH-、HCO3-+H2O![]() H2CO3+OH-,故1L 0.1 mol·L-1 Na2CO3溶液中阴阳离子数之和大于0.3NA,故B错误;
H2CO3+OH-,故1L 0.1 mol·L-1 Na2CO3溶液中阴阳离子数之和大于0.3NA,故B错误;
C、O2和14C2H4的中子数均相同,O2和14C2H4的摩尔质量均为32g/mol,16g O2和14C2H4的混合物的物质的量为:![]() =0.5mol,故该混合物中所含中子数为:0.5mol×16×NAmol-1=8NA,故C正确;
=0.5mol,故该混合物中所含中子数为:0.5mol×16×NAmol-1=8NA,故C正确;
D、N2+3H2![]() 2NH3为可逆反应,故l.5mol H2与0.5mol N2充分反应后,得到NH3的分子数小于NA,故D错误。
2NH3为可逆反应,故l.5mol H2与0.5mol N2充分反应后,得到NH3的分子数小于NA,故D错误。

 阅读快车系列答案
阅读快车系列答案【题目】有A、B、C、D四种易溶于水的白色固体,分别由![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
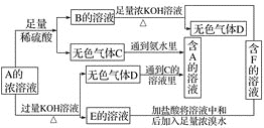
、![]() 中的一种阳离子和一种阴离子组成(同一种离子只存在一种物质中)。某课外小组做了以下实验:①将四种盐各取少量,分别溶于盛有一定量蒸馏水的4支试管中,只有B盐溶液呈蓝色。②分别向4支试管中加入足量稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
中的一种阳离子和一种阴离子组成(同一种离子只存在一种物质中)。某课外小组做了以下实验:①将四种盐各取少量,分别溶于盛有一定量蒸馏水的4支试管中,只有B盐溶液呈蓝色。②分别向4支试管中加入足量稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
(1)根据上述实验事实,推断盐的化学式分别为:A______;D______。
(2)写出下列反应的离子方程式:
①B+D→:______;
③C+HCl→气体:______。
(3)在作实验反思时,有同学提出:如果溶液中同时存在![]() 和
和![]() ,
,![]() 会对
会对![]() 的检验产生干扰。为了确定该溶液中是否存在
的检验产生干扰。为了确定该溶液中是否存在![]() ,该小组同学进行了如下探究实验:
,该小组同学进行了如下探究实验:
实验步骤 | 实验操作 | 实验目的 | 反应的离子方程式 |
第一步 | 向溶液中滴加过量的 | 除去 ______的干扰 | 略 |
第二步 | 向第一步实验后的溶液中滴加______ | 检验 ______的存在 | 略 |