题目内容
14.设NA为阿伏加德罗常数的值.下列说法正确的是( )| A. | 标准状况下,22.4 LH2O中含有的分子数为NA | |
| B. | 1mol•L-1Na2CO3溶液中含有的钠离子数为2NA | |
| C. | 28gN2中含有的原子数为NA | |
| D. | 1molMg与足量稀盐酸反应,转移的电子数为2NA |
分析 A、标况下,水为液体;
B、溶液体积不明确;
C、氮气由氮原子构成;
D、镁与盐酸反应后变为+2价.
解答 解:A、标况下,水为液体,不能根据气体摩尔体积来计算,故A错误;
B、溶液体积不明确,故溶液中钠离子的个数无法计算,故B错误;
C、氮气由氮原子构成,故28g氮气中含有的氮原子的物质的量n=$\frac{m}{M}$=$\frac{28g}{14g/mol}$=2mol,即2NA个,故C错误;
D、镁与盐酸反应后变为+2价,故1mol镁失去2mol电子,即2NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,根据公式的运用和物质的结构来分析是解题关键,难度不大.

练习册系列答案
 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
11.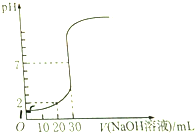 用NaOH溶液滴定10mL盐酸,滴定过程中溶液的pH变化如图.NaOH溶液和盐酸的物质的量浓度(单位:mol•L-1)分别为( )
用NaOH溶液滴定10mL盐酸,滴定过程中溶液的pH变化如图.NaOH溶液和盐酸的物质的量浓度(单位:mol•L-1)分别为( )
 用NaOH溶液滴定10mL盐酸,滴定过程中溶液的pH变化如图.NaOH溶液和盐酸的物质的量浓度(单位:mol•L-1)分别为( )
用NaOH溶液滴定10mL盐酸,滴定过程中溶液的pH变化如图.NaOH溶液和盐酸的物质的量浓度(单位:mol•L-1)分别为( )| A. | 0.12,0.04 | B. | 0.04,0.12 | C. | 0.12,0.06 | D. | 0.03,0.09 |
5.在2A+B?3C+4D反应中,表示该反应速率最快的是( )
| A. | v(A)=0.3mol/(L•s) | B. | v(B)=0.3mol/(L•s) | C. | v(C)=0.3mol/(L•s) | D. | v(D)=1mol/(L•s) |
2.下列气体所含分子数最少的是( )
| A. | 9.0g C2H6 | B. | 标准状况下5.6L 空气 | ||
| C. | 0.75mol N2 | D. | 3.01×1023 个臭氧分子 |
19.一定条件下,在2L密闭容器中发生反应:N2+3H2$?_{催化剂}^{高温、高压}$2NH3,测得1min内,H2的物质的量由3mol减少到1.2mol,则1min内NH3的化学反应速率为( )
| A. | 0.6 mol•L-1•min-1 | B. | 0.9 mol•L-1•min-1 | ||
| C. | 1.2 mol•L-1•min-1 | D. | 1.8 mol•L-1•min-1 |
6.下列做法符合《食品卫生法》的是( )
| A. | 用苏丹红做食品添加剂 | B. | 在奶粉中添加三聚氰胺 | ||
| C. | 用SO2熏制银耳 | D. | 用小苏打发酵面食 |
3.0.8g某气体含有3.01×1022个分子,该气体的摩尔质量为( )
| A. | 16 g•mol-1 | B. | 16 0g•mol-1 | C. | 64 g•mol-1 | D. | 8 g•mol-1 |
4.取pH均等于2的盐酸和醋酸各100L,分别稀释2倍后,再分别加入足量的锌粉,在相同条件下充分反应,有关叙述正确的是( )
| A. | 醋酸与锌粉反应放出的氢气少 | |
| B. | 盐酸和醋酸与锌反应放出氢气一样多 | |
| C. | 醋酸与锌反应速率大 | |
| D. | 盐酸、醋酸与锌反应的速率一样大 |
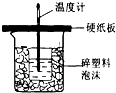 中和热是指酸跟碱发生中和反应生成lmolH2O所放出的热量.某学生想通过测反应过程中所放出的热量来计算中和热.他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题:
中和热是指酸跟碱发生中和反应生成lmolH2O所放出的热量.某学生想通过测反应过程中所放出的热量来计算中和热.他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题: