题目内容
9. 中和热是指酸跟碱发生中和反应生成lmolH2O所放出的热量.某学生想通过测反应过程中所放出的热量来计算中和热.他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题:
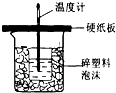
中和热是指酸跟碱发生中和反应生成lmolH2O所放出的热量.某学生想通过测反应过程中所放出的热量来计算中和热.他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题:(1)从实验装置上看,图中尚缺少的一种玻璃用品是环形玻璃搅拌棒,烧杯间满碎塑料泡沫的作用是保温、隔热,减少实验过程中的热量损失.
(2)大烧杯上如不盖硬纸板,则求得的中和热数值偏小(填“偏大”、“偏小”、“无影响”).
(3)实验中改用60mL 0.50mol/L的盐酸跟50mL 0.55mol/L的NaOH溶液进行反应,与上述实验相比,溶液温度升高度数不相等(填“相等”或“不相等”).所求中和热的数值会相等(填“相等”或“不相等”),理由是中和热是指酸跟碱发生中和反应生成lmolH2O所放出的热量,它与酸、碱的用量无关.
分析 (1)根据量热计的构造来判断该装置的缺少仪器;中和热测定实验成败的关键是保温工作;
(2)不盖硬纸板,会有一部分热量散失;
(3)反应放出的热量和所用酸以及碱的量的多少有关,并根据中和热的概念和实质来回答;
解答 解:(1)由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌器;中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是保温、隔热,减少实验过程中的热量损失;
故答案为:环形玻璃搅拌棒;保温、隔热,减少实验过程中的热量损失;
(2)大烧杯上如不盖硬纸板,会有一部分热量散失,求得的中和热数值将会减小;
故答案为:偏小;
(3)反应放出的热量和所用酸以及碱的量的多少有关,若用60mL 0.50mol/L的盐酸跟50mL 0.55mol/L的NaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏大,温度升高度数偏大,但是中和热的均是强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,所以改用60mL 0.50mol/L的盐酸跟50mL 0.55mol/L的NaOH溶液进行上述实验,测得中和热数值相等;
故答案为:不相等;相等;中和热是指酸跟碱发生中和反应生成lmolH2O所放出的热量,它与酸、碱的用量无关.
点评 本题考查学生有关中和热的测定,注掌握实验的原理是解题的关键,注意中和热与酸、碱的物质的量无关,难度不大.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
6.在元素周期表中,金属元素和非金属元素分界线附近能找到( )
| A. | 制半导体元素 | B. | 制农药元素 | ||
| C. | 制催化剂元素 | D. | 制耐高温合金的元素 |
17.为了保护臭氧层,可采取的有效措施是( )
| A. | 减少氟氯烃的排放量 | B. | 减少含铅废气的排放量 | ||
| C. | 减少二氧化硫的排放量 | D. | 减少二氧化碳的排放量 |
4.在抗震救灾中要用大量漂白粉和漂白液杀菌消毒,下列说法中正确的是( )
| A. | 漂白粉是纯净物,漂白液是混合物 | |
| B. | 漂白粉的有效成分是Ca(ClO)2、CaCl2 | |
| C. | 工业上将氯气通入澄清石灰水制取漂白粉 | |
| D. | 漂白粉使用时要让衣物浸泡一段时间是为了让漂白粉与气中的二氧化碳充分反应生成次氯酸 |
14.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,22.4 LH2O中含有的分子数为NA | |
| B. | 1mol•L-1Na2CO3溶液中含有的钠离子数为2NA | |
| C. | 28gN2中含有的原子数为NA | |
| D. | 1molMg与足量稀盐酸反应,转移的电子数为2NA |
18.将H2点燃后插入盛满氯气的集气瓶中,产生的现象是( )
| A. | 爆炸 | B. | 瓶内充满棕色烟 | ||
| C. | 火焰立刻熄灭 | D. | 安静燃烧,产生苍白色火焰 |
19.常温下,下列各组离子在溶液中一定能大量共存的是( )
| A. | 1.0mol/L的KNO3溶液:H+、Fe2+、Cl-、SO42- | |
| B. | 与铝反应产生大量氢气的溶液:Na+、K+、HCO3-、NO3- | |
| C. | pH=12的溶液:K+、Na+、CH3COO-、Br- | |
| D. | 由水电离产生的c(H+)=10-13mol/L的溶液:NH4+、Ba2+、AlO2-、Cl- |