题目内容
【题目】有关物质的转化关系如下图所示(部分物质和条件已略去)。F是最简单的烃,B是最常见的无色液体,A是一种淡黄色固体,G是一种既能溶于强酸又能溶于强碱的白色固体,C由两种短周期元素组成,其摩尔质量为144g·mol1。
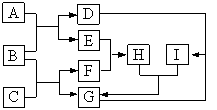
请问答下列问题:
(1)F的电子式为 。
(2)C的化学式为 。
(3)写出A与B反应的化学方程式: 。
(4)写出D溶液与G反应的离子方程式: 。
【答案】(1)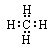 (2)Al4C3
(2)Al4C3
(3)2Na2O2+2H2O=4NaOH+O2↑(4)Al(OH)3+OH-=AlO2-+2H2O
【解析】
试题分析:F是最简单的烃,则F为CH4;B是最常见的无色液体,则B为H2O;A是一种淡黄色固体,且能和H2O发生反应,则A为Na2O2;Na2O2与H2O反应生成NaOH和O2,且E能和CH4发生反应,则E为O2,D为NaOH;G是一种既能溶于强酸又能溶于强碱的白色固体,则G为Al(OH)3;NaOH与Al(OH)3反应生成I,则I为NaAlO2;CH4与O2反应生成H,则H为CO2;C与H2O反应生成CH4和Al(OH)3,则C含有碳元素和铝元素,且其摩尔质量为144g·mol1,则C为Al4C3。
(1)CH4的电子式为
(2)C的化学式为Al4C3;(3)Na2O2与H2O反应生成NaOH和O2,化学方程式为2Na2O2+2H2O=4NaOH+O2↑;(4)NaOH与Al(OH)3反应生成NaAlO2和H2O,离子方程式为Al(OH)3+OH- = AlO2- +2H2O。

 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案【题目】某同学用如下装置进行实验①和②,在相同时间内,记录现象如下(溶液的温度变化均不明显)。
实验装置 | 实验序号 | 电极材料 | 实验现象 |
| ① | 铂 | 两极均产生大量无色气泡, 两极区的溶液均未见白色浑浊 |
② | 石墨 | 两极均产生大量无色气泡, 阴极区未见白色浑浊, 阳极区产生白色浑浊,分离出该白色固体,加酸溶解,产生气泡 |
根据实验现象,下列说法正确的是
A. ①②中,阴极的电极反应式:2H2O-4e == O2↑+ 4H+
B. ②中,白色浑浊的主要成分是Ca(OH)2
C. ②中,产生白色浑浊的主要原因是电解过程消耗水
D. ②中,产生白色浑浊与阳极材料被氧化生成CO32有关