题目内容
进行中和热的测定的装置如图所示.回答下列问题:
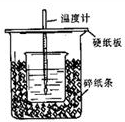
(1)从实验装置中尚缺少的一种玻璃用品是
(2)烧杯间填满碎纸条的作用是
(3)利用该装置测得的中和热数值
(4)某研究小组将装置完善后,把V1 mL 1.0mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).回答下列问题:
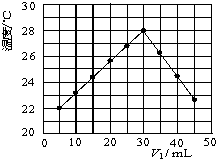
①研究小组做该实验时环境温度
②由题干及图形可知,V1/V2=

(1)从实验装置中尚缺少的一种玻璃用品是
环形玻璃搅拌器
环形玻璃搅拌器
.(2)烧杯间填满碎纸条的作用是
减少实验过程中的热量损失
减少实验过程中的热量损失
.(3)利用该装置测得的中和热数值
偏小
偏小
(填“偏大、偏小、无影响”)(4)某研究小组将装置完善后,把V1 mL 1.0mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).回答下列问题:

①研究小组做该实验时环境温度
低于
低于
(填“高于”、“低于”或“等于”)22℃.②由题干及图形可知,V1/V2=
3:2
3:2
时,酸碱恰好完全中和,此反应所用NaOH溶液的浓度应为1.5
1.5
mol/L.分析:(1)根据量热计的构造来判断该装置的缺少仪器;
(2)中和热测定实验成败的关键是保温工作;
(3)不盖硬纸板,会有一部分热量散失;
(4)从图示观察的起始温度即为实验时的温度;
(5)由图可知,恰好反应时参加反应的盐酸溶液的体积是30mL,由V1+V2=50mL可知,消耗的氢氧化钠溶液的体积为20mL,以此求出两者的体积比值、计算NaOH浓度.
(2)中和热测定实验成败的关键是保温工作;
(3)不盖硬纸板,会有一部分热量散失;
(4)从图示观察的起始温度即为实验时的温度;
(5)由图可知,恰好反应时参加反应的盐酸溶液的体积是30mL,由V1+V2=50mL可知,消耗的氢氧化钠溶液的体积为20mL,以此求出两者的体积比值、计算NaOH浓度.
解答:解:(1)根据量热计的构造可知该装置的缺少仪器是环形玻璃搅拌器,
故答案为:环形玻璃搅拌器;
(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是减少实验过程中的热量损失,
故答案为:减少实验过程中的热量损失;
(3)不盖硬纸板,会有一部分热量散失,温度差减少,测得的中和热数值偏小;
故答案为:偏小;
(4)根据实验结果图2所示内容,可以知道该实验开始时温度一定是低于22℃,
故答案为:低于;
(5)恰好反应时参加反应的盐酸溶液的体积是30mL,由V1+V2=50mL,消耗的氢氧化钠溶液的体积为20mL,所以V1/V2=3/2;设恰好反应时氢氧化钠溶液中溶质的物质的量是n.
HCl+NaOH═NaCl+H2O
1 1
1.0mol?L-1×0.03L n
则n=1.0mol?L-1×0.03L=0.03mol,
所以浓度C=
=1.5mol/L;
故答案为:3:2;1.5.
故答案为:环形玻璃搅拌器;
(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是减少实验过程中的热量损失,
故答案为:减少实验过程中的热量损失;
(3)不盖硬纸板,会有一部分热量散失,温度差减少,测得的中和热数值偏小;
故答案为:偏小;
(4)根据实验结果图2所示内容,可以知道该实验开始时温度一定是低于22℃,
故答案为:低于;
(5)恰好反应时参加反应的盐酸溶液的体积是30mL,由V1+V2=50mL,消耗的氢氧化钠溶液的体积为20mL,所以V1/V2=3/2;设恰好反应时氢氧化钠溶液中溶质的物质的量是n.
HCl+NaOH═NaCl+H2O
1 1
1.0mol?L-1×0.03L n
则n=1.0mol?L-1×0.03L=0.03mol,
所以浓度C=
| 0.03mol |
| 0.02L |
故答案为:3:2;1.5.
点评:本题结合中和反应考查了同学们观察分析问题的能力,以及利用化学方程式计算的能力,比较综合,要认真分析解答.

练习册系列答案
 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目


 mol/L的NaCl溶液,以胶头滴管加水定容时,液面稍超出容量瓶刻度线,反复摇匀后,凹液面最低点恰好与刻度线相切
mol/L的NaCl溶液,以胶头滴管加水定容时,液面稍超出容量瓶刻度线,反复摇匀后,凹液面最低点恰好与刻度线相切