题目内容
【题目】实验是学习化学的基础,某课外兴趣小组在学了苯与液溴的反应以后,对该反应的类型提出了猜想。
(1)甲组认为苯与液溴的反应是加成反应,乙组则认为苯与液溴的反应是___,对此问题你认为该怎样去证明,说出你的方法:___。
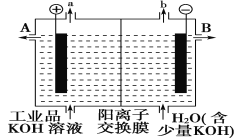
为了证明他们的猜想是否正确,按照如图的实验装置(夹持装置省略)进行实验。

(2)比较装置Ⅰ和装置Ⅱ,选择___(装置Ⅰ或装置Ⅱ),装置Ⅱ的A中CCl4溶液的作用是___。
(3)装有苯和铁粉的仪器名称是___,B集气瓶的作用是___,若试管中出现___现象乙组猜想正确。
(4)写出铁与液溴反应的化学方程式___,苯和液溴反应的化学方程式___。
(5)简要叙述除去溴苯中溴的方法:___。
【答案】取代反应 检验是否有HBr生成,若有HBr生成,则是取代反应,反之是加成反应。 装置Ⅱ 吸收溴蒸气和苯蒸气,防止对实验干扰 蒸馏烧瓶 安全瓶,防倒吸 淡黄色沉淀 2Fe+3Br2=2FeBr3 ![]() +Br2
+Br2![]() +HBr 将粗溴苯倒入分液漏斗中滴加Na2SO3溶液,振荡,至有机层无色为止,分液
+HBr 将粗溴苯倒入分液漏斗中滴加Na2SO3溶液,振荡,至有机层无色为止,分液
【解析】
(1)苯与液溴可能发生取代反应或加成反应;如果发生取代反应,需要验证生成物的性质;
(2)要想验证谁的猜想正确,需要验证生成物,用硝酸银验证溴化氢,所以选择装置Ⅱ,应用四氯化碳的性质分析它起的作用;
(3)按照仪器的名称写出装置的名称,B装置起到缓冲的作用,取代反应发生后的生成物溴化氢用硝酸银检验,根据反应说出化学方程式;
(4)铁和液溴发生反应生成溴化铁,苯和液溴发生取代反应生成溴苯和溴化氢,形成化学方程式;
(5)利用溴的氧化性,设计实验;
(1)甲组同学认为苯和液溴发生的是加成反应,乙组同学认为苯和液溴发生的是取代反应,苯和液溴发生取代反应的生成物为溴苯和溴化氢,检验是否有HBr生成,若有HBr生成,则是取代反应,反之是加成反应。
(2)甲和乙的猜想到底是谁正确,需要验证产物溴化氢,可以用硝酸银检验溴化氢,故选择装置Ⅱ,苯和溴在铁做催化剂存在的条件下反应生成溴苯和溴化氢,苯和溴蒸气容易随着产物一起逸出,故用四氯化碳吸收溴蒸气和苯蒸气,防止对实验干扰;
(3)装有苯和铁粉的仪器名称是蒸馏烧瓶,B集气瓶的作用是安全瓶,防倒吸,若按照乙的观点,则会有溴化氢生成,溴化氢与硝酸银反应生成溴化银和硝酸,溴化银是淡黄色沉淀,故有淡黄色沉淀生成,则证明乙的观点正确;
(4)铁和液溴发生反应生成溴化铁,溴的氧化性较强,苯和液溴发生取代反应生成溴苯和溴化氢,形成化学方程式;2Fe+3Br2=2FeBr3,![]() +Br2
+Br2![]() +HBr;
+HBr;
(5)若溴苯中有溴,溴可以和亚硫酸钠溶液反应而除去,溴苯和亚硫酸钠溶液不互溶,可以将粗溴苯倒入分液漏斗中滴加Na2SO3溶液,振荡,至有机层无色为止,分液;

 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案 培优三好生系列答案
培优三好生系列答案