题目内容
【题目】如下图所示,试管中集满了干燥的氯气,胶头滴管中装有供反应的足量浓氨水,滴入浓氨水,开始时试管内发生如下氧化还原反应:NH3+Cl2 →N2+HCl并产生红光和白烟,请根据以上反应现象回答下列问题:
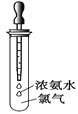
(1)标志反应全部完成的现象是________________________。
(2)反应完成后,将试管浸入水中并倒立着试管,取下滴管,有水进入试管。在室温时,进入试管内的水约占试管容积的_________。
(3)反应中生成的白烟是:_____________________________。
(4)写出试管中反应的化学方程式:___________________________
【答案】 不再产生红光和白烟 2/3 NH4Cl 2NH3+3Cl2 =N2+6HCl、HCl+NH3=NH4Cl
【解析】试题分析:由题意知因发生反应8NH3+3Cl2=6NH4Cl+N2时放出大量的热而产生红光和白烟。当不再产生红光和白烟时表明不再放出大量的热,此时反应已经完成。由反应方程式可知,反应产生的N2为参加反应的Cl2的物质的量的1/3,故进入试管的水的体积约为试管容积的2/3。显然白烟为NH4Cl。
解析:根据以上分析(1)标志反应全部完成的现象是不再产生红光和白烟。
(2)由反应方程式可知,反应产生的N2为参加反应的Cl2的物质的量的1/3,故进入试管的水的体积约为试管容积的2/3。
(3)反应中生成的白烟是:NH4Cl。
(4)试管中反应的化学方程式:2NH3+3Cl2 =N2+6HCl、HCl+NH3=NH4Cl

练习册系列答案
相关题目