题目内容
【题目】固定和利用CO2能有效地利用资源,并减少空气中的温室气体。工业上有一种用CO来生产甲醇燃料的方法: CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示a,b,c,d括号内数据表示坐标。
CH3OH(g)+H2O(g)。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示a,b,c,d括号内数据表示坐标。
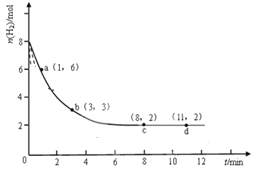
(1)0-a,a-b,b-c,c-d四段中,平均反应速率最大的时间段是 ,该时间段内H2的平均反应速率是 。
(2)a点正反应速率_______(填大于、等于或小于)逆反应速率。
(3)平衡时CO2的转化率是 ;反应前后容器内的压强比是 。
【答案】(1)0—a; 1mol/(L min);
(2)大于
(3)33.3 % 或 33.33% 7∶5
【解析】
试题分析:(1)由图像知反应是从正反应方向开始直至建立平衡。当其他条件不变时,反应物的浓度越大,化学反应速率越快,故在0~a,a~b,b~c,c~d四段中,平均反应速率最大的时间段是0~a,该时间段内H2的物质的量变化为2mol,容器的体积为2L,根据公式v=△n/△tV计算H2的平均反应速率是![]() =1mol/(L min)。
=1mol/(L min)。
(2)由图像可判断a点时反应还没有达到化学平衡,反应正向进行,则正反应速率大于逆反应速率。
(3)根据题给信息知反应开始时c(CO2)=3mol/L,c(H2)=4mol/L,c(CH3OH)=0mol/L,c(H2O)= 0mol/L,当达到化学平衡时根据图像可知c(H2)=1mo/L,c(CO2)=2mol/L,c(CH3OH)=1mol/L,c(H2O)=1mol/L。则平衡时CO2的转化率为:(1mol/L÷3mol/L)×100﹪=33.3﹪;等温等体积的条件下,容器内的压强之比等于气体的物质的量之比等于![]() =7:5。
=7:5。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
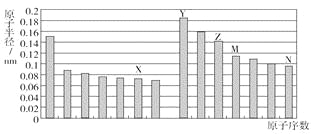
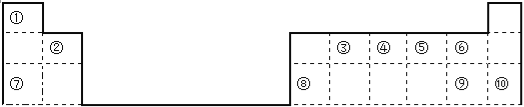
小学生10分钟应用题系列答案【题目】元素周期表是学习化学的重要工具,它隐含着许多信息和规律。下面是八种短周期元素的相关信息(已知铍的原子半径为0.089 nm)
元素代号 | A | B | C | D | E |
原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.074 |
主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
F原子中无中子,G最高正价数与负价数相等,且最外层电子数是次外层的二倍,H元素单质焰色反应呈黄色。
(1)C元素在元素周期表中的位置 。B形成的简单离子的结构示意图 。
(2)上述八种元素的最高价氧化物对应的水化物中酸性最强的是 (填化学式)。
(3)用电子式表示A、D形成化合物的过程: 。
(4)H、E形成原子个数比为1∶1的化合物中所含化学键类型为 。
(5)GE2的电子式为 ,F与G形成的最简单的化合物的结构式为 。
(6)E的氢化物比C的氢化物的熔沸点高的原因是 。
(7)A、B、C、E原子半径由大到小的顺序为(用元素符号表示) 。