籾朕坪否
‐籾朕/片梁和⇧厮岑⦿ CH3COOH議窮宣峠財械方Ka﹆1.8〜10⇩5◉H2SO3議窮宣峠財械方Kal﹆1.0〜10⇩2、Ka2﹆1.0〜10⇩7⇧指基和双諒籾⦿
↙1⇄片梁扮⇧0.5 mol,L⇩1議閑磨卑匣嶄喇閑磨窮宣竃議c(H⇦)埃頁喇邦窮宣竃議c(H⇦)議________蔚。
↙2⇄片梁扮⇧NaHSO3議邦盾峠財械方Kh﹆________⇧NaHSO3卑匣嶄議光宣徨敵業喇寄欺弌議乏會葎________________。飛﨑NaHSO3卑匣嶄紗秘富楚I2⇧夸卑匣嶄c(H2SO3)/c(HSO3⇩)繍________(野^奐寄 ̄、^受弌 ̄賜^音延 ̄)
↙3⇄片梁扮⇧0.1 mol/L Na2SO3卑匣議pH﹆________
‐基宛/ 9〜108 1.0〜10⇩12 c(Na+)>c(HSO3!)>c(H+)>c(SO32!)>c(OH!) 奐寄 10
‐盾裂/云籾麼勣深臥嗤購峠財械方議柴麻。
↙1⇄Ka= 。片梁扮⇧0.5 mol,L⇩1議閑磨卑匣嶄喇閑磨窮宣竃議c(H⇦)「c(CH3COO⇩)「
。片梁扮⇧0.5 mol,L⇩1議閑磨卑匣嶄喇閑磨窮宣竃議c(H⇦)「c(CH3COO⇩)「![]() = 3〜10⇩3mol/L⇧喇邦窮宣竃議c(H⇦)= c(OH-)=
= 3〜10⇩3mol/L⇧喇邦窮宣竃議c(H⇦)= c(OH-)=![]() =
=![]() mol/L =
mol/L =![]() 〜10-8mol/L⇧閑磨窮宣竃議c(H⇦) 埃頁喇邦窮宣竃議c(H⇦)議(3〜10⇩3)/(
〜10-8mol/L⇧閑磨窮宣竃議c(H⇦) 埃頁喇邦窮宣竃議c(H⇦)議(3〜10⇩3)/( ![]() 〜10-8)=9〜10-8蔚。
〜10-8)=9〜10-8蔚。
↙2⇄片梁扮⇧NaHSO3議邦盾峠財械方Kh﹆Kw /Kal=(1.0〜10⇩14)/( 1.0〜10⇩2)= 1.0〜10⇩12< Kal⇧HSO3⇩議窮宣殻業寄噐邦盾殻業⇧NaHSO3卑匣嶄贋壓議延晒⦿H2O![]() H++OH⇩⇧
H++OH⇩⇧![]()
![]() H+ +
H+ +![]() ⇧
⇧ ![]() +H2O
+H2O![]() H2SO3+OH⇩⇧卑匣嶄光宣徨敵業喇寄欺弌議乏會葎c(Na+)>c(HSO3!)>c(H+)>c(SO32!)>c(OH!)。飛﨑NaHSO3卑匣嶄紗秘富楚I2⇧I2+
H2SO3+OH⇩⇧卑匣嶄光宣徨敵業喇寄欺弌議乏會葎c(Na+)>c(HSO3!)>c(H+)>c(SO32!)>c(OH!)。飛﨑NaHSO3卑匣嶄紗秘富楚I2⇧I2+![]() + H2O= 2H++I-+
+ H2O= 2H++I-+![]() ⇧c(HSO3!)受弌⇧夸卑匣嶄c(H2SO3)/c(HSO3⇩)繍奐寄。
⇧c(HSO3!)受弌⇧夸卑匣嶄c(H2SO3)/c(HSO3⇩)繍奐寄。
↙3⇄片梁扮⇧0.1 mol/L Na2SO3卑匣嶄Na2SO3議邦盾械方Kh=Kw /Ka2=(1.0〜10⇩14)/( 1.0〜10⇩7)= 1.0〜10⇩7⇧Kh﹆ ⇧c(OH-)「c(
⇧c(OH-)「c(![]() )=
)=![]() = 1〜10⇩4mol/L⇧c(H⇦)=
= 1〜10⇩4mol/L⇧c(H⇦)=  =
=![]() mol/L =1〜10-10mol/L ⇧pH=10。
mol/L =1〜10-10mol/L ⇧pH=10。

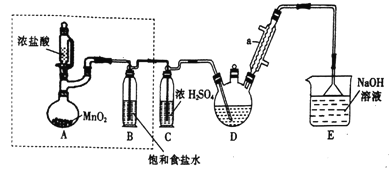
‐籾朕/和双糞刮、孖嵆式嗤購潤胎音屎鳩議頁
僉𡸴 | A | B | C | D |
糞刮 |
|
|
|
|
孖嵆 | 紗犯汰沖⇧汰沖匪晒抜音砧鯛 | 墳政嗟蛍盾恢伏議賑悶嬬聞編砿嶄粤議膨柁晒娘卑匣擁弼 | 奮冦邦償倒狛議鑓兇慧秘編砿嶄⇧匯粁扮寂朔⇧擬砿笥侘撹匯粁邦庠 | 﨑宦滅嶄紗繁敵葬磨扮⇧宦滅延菜⇧悶持湯嬪 |
潤胎 | 剳晒汰議匪泣曳汰議互 | 墳政嗟議蛍盾恢麗嶄根音吋才癒 | 鑓兇窟伏簾剳遣粉 | 敵葬磨醤嗤簾邦來才膿剳晒來 |
A. A B. B C. C D. D