题目内容
11.将10克Na2O2、Na2O、Na2CO3、NaOH混合物与100克质量分数3.65%的盐酸恰好反应,蒸干溶液,最终得固体质量为( )| A. | 5.85 g | B. | 11.7 g | C. | 8 g | D. | 15.5 g |
分析 Na2O2、Na2O、Na2CO3、NaOH的混合物与盐酸恰好反应,所得溶液中溶质为NaCl,溶液蒸干所得固体为NaCl,根据氯原子守恒有n(NaCl)=n(HCl),根据m(溶质)=m(溶液)×w(溶质)计算m(HCl),进而计算n(NaCl),再根据m=nM计算NaCl的质量.
解答 解:Na2O2、Na2O、Na2CO3、NaOH的混合物与盐酸恰好反应,所得溶液中溶质为NaCl,溶液蒸干所得固体为NaCl,根据氯原子守恒有n(NaCl)=n(HCl),
盐酸中m(HCl)=100g×3.65%=3.65g,n(NaCl)=n(HCl)=$\frac{3.65g}{36.5g/mol}$=0.1mol,故得到NaCl的质量=0.1mol×58.5g/mol=5.85g,
故选A.
点评 本题考查混合物的有关计算,题目涉及反应过程比较多,但过程不复杂,侧重考查学生的解题方法技巧与思维能力,注意利用守恒思想进行解答,利用常规方法无法解答,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.课本实验中出现的“草酸溶液与酸性高锰酸钾溶液反应,其反应速率逐渐加快”.经分析某粒子具有催化作用,该粒子是( )
| A. | H+ | B. | SO42- | C. | MnO4- | D. | Mn2+ |
2.下列叙述中正确的是( )
| A. | 1 mol任何气体的体积都约为22.4L | |
| B. | 在标准状况下某气体的体积约为22.4L,则该气体约含有6.02×1023个分子 | |
| C. | 16.0gCuSO4•5H2O溶于水配成1L溶液,其物质的量浓度为1mol/L | |
| D. | 标准状况下,22.4LHCl气体溶于1L水中,所得溶液浓度为1mol/L |
6.下列酒类,其中酒精含量最高的是( )
| A. | 啤酒 | B. | 白酒 | C. | 葡萄酒 | D. | 黄酒 |
16.下列叙述正确的是( )
| A. | 1 molOH- 的质量为18g/mol | |
| B. | CO2 的摩尔质量为44g | |
| C. | 任何物质的摩尔质量等于它的相对原子质量或相对分子质量 | |
| D. | 一个钠原子的质量约等于$\frac{23}{6.02×1{0}^{23}}$ g |
3.如图所示,a、b是石墨电极,通电一段时间后,b极附近溶液显红色.下列说法正确的是( )
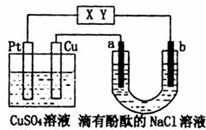

| A. | X极是电源负极,Y极是电源正极 | |
| B. | Pt极上有6.4gCu析出时,b极产生2.24L(标准状况)气体 | |
| C. | a极的电极反应式为:2C1--2e-═C12↑ | |
| D. | 电解过程中 CuSO4溶液的pH逐渐增大 |
20.把9mL NO气体装入试管,倒立于水槽中,逐渐通入O2,当试管中剩余气体为3mL时,通入O2的体积可能是( )
| A. | 9 mL | B. | 6.75 mL | C. | 4.5 mL | D. | 3 mL |