题目内容
根据元素周期律特点,Na、Mg、Al三种元素从左到右描述正确的是( )
| A、金属性依次增强 |
| B、最外层电子数依次增多 |
| C、原子半径依次增大 |
| D、最高正价依次减小 |
考点:同一周期内元素性质的递变规律与原子结构的关系
专题:元素周期律与元素周期表专题
分析:同周期元素从左到右,半径逐渐减小,元素的金属性逐渐减弱,对应单质的还原性逐渐减弱;元素的非金属性、电负性逐渐增强,元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,以此解答该题.
解答:
解:A.同周期元素从左到右,金属性依次减弱,故A错误;
B.Na、Mg、Al三种元素最外层电子数依次为1、2、3,故B正确;
C.同周期元素从左到右,半径逐渐减小,故C错误;
D.Na、Mg、Al三种元素最外层电子数依次为1、2、3,最高正价依次为+1、+2、+3,故D错误.
故选B.
B.Na、Mg、Al三种元素最外层电子数依次为1、2、3,故B正确;
C.同周期元素从左到右,半径逐渐减小,故C错误;
D.Na、Mg、Al三种元素最外层电子数依次为1、2、3,最高正价依次为+1、+2、+3,故D错误.
故选B.
点评:本题考查同周期元素的性质的递变规律,为高频考点,侧重有学生的分析能力的考查,题目难度不大,注意相关基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列微粒的结构示意图中氧离子结构示意图的是( )
A、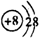 |
B、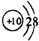 |
C、 |
D、 |
互为同分异构体的一组物质是( )
| A、H2O和H2O2 |
| B、35Cl和37Cl |
| C、氧气(O2)与臭氧(O3) |
| D、乙醇(CH3CH2OH)和甲醚(CH3OCH3) |
在一定条件下,下列物质不能和二氧化硅反应的是( )
①焦炭 ②纯碱 ③碳酸钙 ④氢氟酸 ⑤硝酸 ⑥氢氧化钾 ⑦氧化钙 ⑧氮气.
①焦炭 ②纯碱 ③碳酸钙 ④氢氟酸 ⑤硝酸 ⑥氢氧化钾 ⑦氧化钙 ⑧氮气.
| A、③⑤⑦⑧ | B、⑤⑦⑧ |
| C、⑤⑧ | D、⑤ |
下列说法中错误的是( )
| A、当中心原子的配位数为6时,配合单元常呈八面体空间结构 |
| B、SO3为平面正三角形结构 |
| C、已知[Cu(NH3)2]2+的中心原子采用sp杂化,则它们的空间构型为直线型 |
| D、配位数为4的配合物均为正四面体结构 |
用铂作电极,KOH溶液作电解质溶液,分别向两极通入CH4和O2,即产生电流,称为甲烷燃料电池.已知甲烷燃料电池的总反应为CH4+2O2+2OH-═CO32-+3H2O,下列有关说法中错误的是( )
| A、CH4在负极上反应 |
| B、放电过程中电解质溶液的碱性不变 |
| C、此电池属于环境友好电池 |
| D、可判断正极反应式为:2O2+8e-+4H2O═8OH- |
有主族元素X、Y,X的原子序数为a,X+比Y2-少8个电子,则Y的原子序数为( )
| A、a+4 |
| B、a+5 |
| C、a+6 |
| D、a+7 |
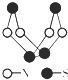 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )| A、该物质的分子式为SN |
| B、该物质的晶体中微粒间作用力有2种 |
| C、该物质具有很高的熔、沸点 |
| D、该物质与化合物S2N2互为同素异形体 |
下列说法中正确的是( )
| A、凡能发生银镜反应的有机物一定是醛 |
| B、在氧气中燃烧时只生成CO2和H2O的物质一定是烃 |
| C、苯酚有弱酸性,俗称石炭酸,因此它是一种羧酸 |
| D、在酯化反应中,羧酸脱去羧基中的羟基,醇脱去羟基中的氢而生成水和酯 |