题目内容
【题目】安全气囊做为车身被动安全性的辅助配置,日渐受到人们的重视,其设计原理为6NaN3+Fe2O3=3Na2O+2Fe+9N2↑,请回答下列问题:
(1)以上5种物质中属于电解质的是 ,属于盐类的是 。
(2)NH3分子的空间构型是 ,NH3分子可以作配体和铜离子形成四氨合铜离子[Cu(NH3)4]2+,请写出[Cu(NH3)4]2+的结构式 (注明配位键)。
(3)N和O的气态氢化物中,较稳定的是 (写化学式),氧的同族元素(包括O)的最简单氢化物中沸点最低的是 (写化学式)。
(4)写出一个与NaN3中N3-具有相似空间构型的等电子体(分子或离子) 。
【答案】(1)NaN3 、Fe2O3 、Na2O,NaN3;
(2)三角锥形,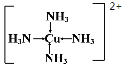 ;
;
(3)H2O,H2S;(4)CO2、CS2、CNO-、SCN-、N2O。
【解析】
试题分析:(1)电解质:在水溶液中或熔融状态下能够导电化合物,属于电解质为酸、碱、盐、金属氧化物等,因此属于电解质为NaN3、Fe2O3、Na2O,属于盐的是NaN3;(2)氨气分子中孤电子对数为(5-3×1)/2=1,价层电子数为4,则空间构型为三角锥,铜离子提供空轨道,氨气中N提供孤电子对,则结构式为: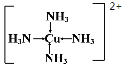 ;(3)同周期从左向右非金属性增强,非金属性越强,其氢化物越稳定,即H2O最稳定,H2O之间含有分子间氢键,沸点高,结构和组成相似,相对分子质量越大,分子间作用力越大,熔沸点越高,因此沸点最低的是H2S;(4)等电子体:原子总数相等、价电子总数相等,因此N3-的等电子体为CO2、CS2、CNO-、SCN-、N2O。
;(3)同周期从左向右非金属性增强,非金属性越强,其氢化物越稳定,即H2O最稳定,H2O之间含有分子间氢键,沸点高,结构和组成相似,相对分子质量越大,分子间作用力越大,熔沸点越高,因此沸点最低的是H2S;(4)等电子体:原子总数相等、价电子总数相等,因此N3-的等电子体为CO2、CS2、CNO-、SCN-、N2O。

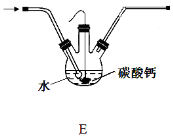
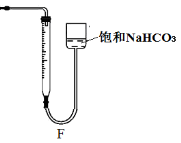
【题目】七铝十二钙 (12CaO·7Al2O3)是一种新型的超导材料和发光材料,它是用AlC13溶液溶解一定量的CaCO3形成溶液,再用氨水沉淀,然后锻烧沉淀制备。工业上制备AlC13溶液用图示流程(已知A1C13易升华)。

(1)轻烧后的气体用水处理前导气管为何要保温?
(2)用水处理添加的试剂X是 ,其目的是 。
(3)AlC13溶液溶解CaCO3时,要控制碳酸钙和AlC13的量,要求n(CaCO3): n(A1C13)> 12:14,其原因是 。用氨水沉淀、过滤后的滤液主要成分是 。
(4)以工业碳酸钙(含有少量A12O3、Fe3O4杂质)生产二水合氯化钙(CaC12·2H2O)的方法为:将工业碳酸钙溶于盐酸,加入双氧水, 。(实验中需用到的试剂和仪器有:盐酸,双氧水,氢氧化钙,冰水,pH计)。
已知:几种离子生成氢氧化物沉淀pH(开始沉淀的pH按金属离子浓度为1.0mol/L计算)
开始沉淀的pH | 完全沉淀的pH | |
Fe3+ | 1.1 | 3.2 |
Al3+ | 3.5 | 4.7 |
补全实验步骤: 冰水洗涤,干燥,得到CaC12·2H2O。