题目内容
9.下列有关物质结构的说法正确的是( )| A. | 78 g Na2O2晶体中所含阴、阳离子个数均为4NA | |
| B. | 3.4 g氨气中含有0.6NA个N-H键 | |
| C. | Na2O2的电子式为: | |
| D. | PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构 |
分析 A.根据过氧化钠的物质的量以及1个过氧化钠中含有2个阳离子和1个阴离子;
B.根据氨气的物质的量以及1个氨气中含有3个N-H键;
C.过氧化钠为离子化合物,电子式中需要标出所带电荷;
D.对于共价化合物元素化合价绝对值+元素原子的最外层电子层=8,则该元素原子满足8电子结构;
解答 解:A.78g Na2O2晶体的物质的量为:$\frac{78g}{78g/mol}$=1mol,1个过氧化钠中含有2个阳离子和1个阴离子,78g Na2O2晶体中所含阴、阳离子个数分别为NA、2NA,故A错误;
B.3.4g氨气的物质的量为:$\frac{3.4g}{17g/mol}$=0.2mol,1个氨气中含有3个N-H键,所以3.4g氨气中含有0.6NA个N-H键,故B正确;
C.Na2O2是钠离子和过氧根离子构成的离子化合物,钠离子失电子形成阳离子,氧原子得到电子形成过氧根阴离子,过氧化钠正确的电子式为: ,故C错误;
,故C错误;
D.PCl3中P元素化合价为+3价,P原子最外层电子数是5,3+5=8,则P原子满足8电子结构,Cl元素化合价绝对值为1,其最外层电子数是7,1+7=8,则Cl原子满足8电子结构;BF3中B元素化合价为+3,Be原子最外层电子数为3,所以3+3=6,分子中Be原子不满足8电子结构,故D错误;
故选B.
点评 本题阿伏伽德罗常数的计算与判断、电子式的书写等知识,题目难度中等,注意掌握物质的量与阿伏伽德罗常数、摩尔质量等物理量之间的关系,明确电子式的概念及书写原则.

练习册系列答案
相关题目
4.能正确表示下列反应的离子方程式是( )
| A. | 少量CO2通入苯酚钠溶液中:C6H5O-+CO2+H2O═C6H5OH+HCO3- | |
| B. | NaHCO3溶液中加入稀HCl:CO32-+2H+═CO2↑+H2O | |
| C. | AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O═AlO2-+2H2O | |
| D. | 醋酸溶液中加入少量CaCO3固体:CaCO3+2H+═Ca2++H2O+CO2↑ |
14.下列过程没有发生化学反应的是( )
| A. | 用铂丝蘸取NaC1溶液于酒精灯火焰上灼烧,火焰呈黄色 | |
| B. | SO2使品红溶液褪色 | |
| C. | 用食醋清洗热水瓶内的水垢 | |
| D. | 向装有Fe(NO3)2溶液的试管中滴加稀H2SO4,在试管口观察到红棕色气体 |
1.下列各组离子既能与镁粉反应,又能大量共存,且其溶液为无色溶液的是( )
| A. | Ca2+、Cl-、$MnO_4^-$、Na+ | B. | K+、Cl-、$SO_4^{2-}$、H+ | ||
| C. | OH-、Na+、Al3+、I- | D. | H+、Cl-、Ba2+、Ag+ |
16.电子构型为[Ar]3d104s2的元素属于( )
| A. | s区 | B. | p区 | C. | d 区 | D. | ds区 |

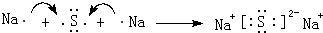 .
.
 现有反应:A、CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
现有反应:A、CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑