题目内容
13.下列说法正确的是( )| A. | 因为SO2具有漂白性,所以它能使品红溶液、溴水、KMnO4溶液、石蕊试液褪色 | |
| B. | 能使品红褪色的不一定是SO2 | |
| C. | SO2、漂白粉、活性炭、Na2O2都能使红墨水褪色,其原理相同 | |
| D. | 盐酸能使滴有酚酞的NaOH溶液褪色,所以盐酸也有漂白性 |
分析 二氧化硫具有漂白性,使品红褪色,而具有还原性,与溴水、高锰酸钾、硝酸等发生氧化还原反应;具有酸性氧化物的通性,以此来解答.
解答 解:A.SO2具有漂白性,它能使品红溶液褪色,具有还原性使溴水、酸性高锰酸钾溶液褪色,二氧化硫使石蕊变红,故A错误;
B.二氧化硫、次氯酸等物质都能使品红溶液褪色,所以能使品红溶液褪色的物质不一定是SO2,故B正确;
C.漂白粉和过氧化钠的漂白性是利用其氧化性,活性炭的漂白性是利用其吸附性,二氧化硫的漂白性是因为和有色物质反应生成无色物质,所以其漂白原理不一定相同,故C错误;
D.盐酸与氢氧化钠发生中和反应,中性、酸性条件下酚酞为无色,盐酸不具有漂白性,故D错误.
故选B.
点评 本题考查二氧化硫的性质,为高频考点,综合考查元素化合物知识,把握漂白原理及发生的氧化还原反应为解答的关键,题目难度不大.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
3.已知浓硫酸与木炭粉在加热条件下的化学方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑十CO2↑2H2O↑.酸性KMnO4溶液可以吸收SO2,试用如图所示各装置设计一个实验,验证上述反应所产生的各种产物.
(1)这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号):④→②→①→③.
(2)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色.A瓶溶液的作用是验证产物的SO2,B瓶溶液的作用是将SO2全部氧化吸收,C瓶溶液的作用是确定产物中SO2已被B瓶溶液全部氧化.
(3)装置②中所加的固体药品是无水硫酸铜,可确证的产物是水蒸气,确定装置②在整套装置中位置的理由是产物气流通过①、③时会带出水蒸气,所以②必须在①、③之间.
(4)装置③中所盛溶液是澄清石灰水,可验证的产物是CO2.
| 编号 | ① | ② | ③ | ④ |
| 装置 | 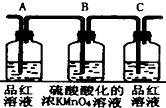 | 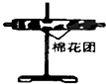 |  | 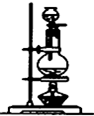 |
(2)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色.A瓶溶液的作用是验证产物的SO2,B瓶溶液的作用是将SO2全部氧化吸收,C瓶溶液的作用是确定产物中SO2已被B瓶溶液全部氧化.
(3)装置②中所加的固体药品是无水硫酸铜,可确证的产物是水蒸气,确定装置②在整套装置中位置的理由是产物气流通过①、③时会带出水蒸气,所以②必须在①、③之间.
(4)装置③中所盛溶液是澄清石灰水,可验证的产物是CO2.
4.在标准状况下,有一氧化碳和二氧化碳的混合气体5.6L.如果一氧化碳的质量为5.6g,则二氧化碳的质量为( )
| A. | 4.4g | B. | 3.3g | C. | 1.1g | D. | 2.2g |
18.工业上制取氧气的主要方法是( )
| A. | 加热氯酸钾 | B. | 加热高锰酸钾 | C. | 电解水 | D. | 分离空气 |
5.已知Cl2与NaOH能发生反应:Cl2+2NaOH═NaCl+NaClO+H2O,则下列有关说法正确的是( )
| A. | 题中氯的化合价变化为:0→-1,被还原,NaOH是还原剂 | |
| B. | 题中氯的化合价变化为:0→+1,被氧化,NaOH是氧化剂 | |
| C. | NaOH既是氧化剂,又是还原剂 | |
| D. | Cl2→Cl-的变化不一定是加还原剂才能实现 |
2.在同温同压下,下列各组热化学方程式中,Q2>Q1的是( )
| A. | 2H2(g)+O2(g)=2H2O(g)△H=-Q1kJ/mol; 2H2(g)+O2(g)=2H2O(g))△H=-Q2kJ/mol | |
| B. | S(g)+O2(g)=SO2(g)△H=-Q1kJ/mol; S(s)+O2(g)=SO2(g))△H=-Q2kJ/mol | |
| C. | C(s)+$\frac{1}{2}$O2(g)=CO2(g))△H=-Q1kJ/mol; C(s)+O2(g)=CO(g))△H=-Q2kJ/mol | |
| D. | H2(g)+Cl2(g)=2HCl(g)△H=-Q1kJ/mol; $\frac{1}{2}$H2(g)+Cl2(g)=HCl(g))△H=-Q2kJ/mol |
 .
.
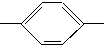 CH═N
CH═N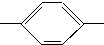 CH2CH2CH2CH3 MBBA
CH2CH2CH2CH3 MBBA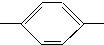 CHO 醛A
CHO 醛A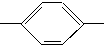 NH2 胺B
NH2 胺B NH2、CH3CH2CH2CH2
NH2、CH3CH2CH2CH2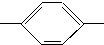 NH2、CH3CH2CH(CH3)
NH2、CH3CH2CH(CH3)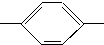 NH2、(CH3)3C
NH2、(CH3)3C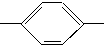 NH2.
NH2.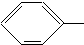 COOCH3、
COOCH3、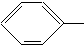 OOCCH3、HCOO
OOCCH3、HCOO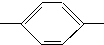 CH3、
CH3、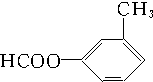 、
、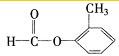 、
、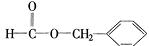 .
.