题目内容
【题目】A是用途最广的金属,B、C是两种常见气体单质,E溶液为常见强酸,D溶液中滴加KSCN溶液显血红色,它们相互转化关系如图所示。
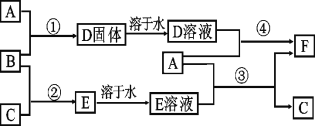
请回答:
(1)写出B物质的化学式:_______;F的化学名称:_______。
(2)写出第②步C在B中燃烧的反应现象:_______。
(3)写出第④步反应的化学反应方程式_______。
(4)F溶液中滴入NaOH溶液可能产生的实验现象是____,写出该反应的化学方程式_____________________ 。
【答案】Cl2 氯化亚铁 产生苍白色火焰,瓶口有白雾产生 Fe+2FeCl 3=3FeCl2 先产生白色沉淀,后立即变成灰绿色,最后变成红褐色 4Fe(OH)2+2 H2O + O2 =4Fe(OH)3
【解析】
B、C是气体单质,B、C反应生成E,E溶液为常见强酸,所以E溶液是盐酸;A是用途最广的金属,D溶液中滴加KSCN溶液显血红色,A是铁,铁与盐酸反应生成氯化亚铁和氢气,则C是氢气、B是氯气,D是氯化铁,F是氯化亚铁。
根据以上分析,(1)B是氯气,化学式是Cl2;F是氯化亚铁。
(2)C是氢气、B是氯气,氢气在氯气中燃烧的反应现象是产生苍白色火焰,瓶口有白雾产生。
(3)第④步反应是氯化铁和铁反应,反应的化学反应方程式是Fe+2FeCl 3=3FeCl2。
(4)氯化亚铁溶液中滴入NaOH溶液,生成白色氢氧化亚铁沉淀,氢氧化亚铁被氧气氧化为红褐色氢氧化铁,可能产生的实验现象是先产生白色沉淀,后立即变成灰绿色,最后变成红褐色,反应的化学方程式是4Fe(OH)2+2 H2O + O2 =4Fe(OH)3。

【题目】CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标。
(1)250℃时,以镍合金为催化剂,向4 L密闭容器中通入6 mol CO2、6 mol CH4,发生如下反应:CO2(g)+CH4(g)![]() 2CO(g)+2H2(g)。平衡体系中各组分体积分数如下表:
2CO(g)+2H2(g)。平衡体系中各组分体积分数如下表:
物质 | CH4 | CO2 | CO | H2 |
体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |
①此温度下该反应的平衡常数K=___________。
②已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3 kJ·mol-1
CO(g)+H2O(g)=CO2(g)+H2(g) △H=2.8 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H=-566.0 kJ·mol-1
反应CO2(g)+CH4(g)![]() 2CO(g)+2H2(g) 的△H=______________;
2CO(g)+2H2(g) 的△H=______________;
③在不同温度下催化剂的催化效率与CO的生成速率如右图所示。t1~t2℃时,温度升高而CO的生成速率降低的原因是___________________________________;
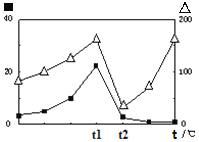 (代表CO的生成速率,■代表催化剂的催化效率)
(代表CO的生成速率,■代表催化剂的催化效率)
④为了提高该反应中CH4的转化率,可以采取的措施是_____________________;
⑤若再向容器中同时充入2.0 mol CO2、6.0 mol CH4、4.0 molCO 和8.0 molH2,则上述平衡向__________(填“正反应”或“逆反应”)方向移动。
(2)以CO2为原料可以合成多种物质。
①可降解二氧化碳聚合物是由CO2加聚而成,写出其结构简式:_____________;
②以氢氧化钾水溶液作电解质进行电解,CO2在铜电极上可转化为甲烷,该电极反应方程式为______。