题目内容
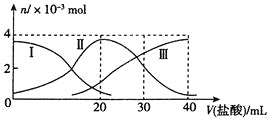
【题目】常温下,向20mL0.2molL-1Na2A溶液中滴加0.2molL-1的盐酸,溶液中含A元素的各微粒物质的量如图所示,下列说法错误的是( )
A.Na2A溶液中,c(A2-)+c(HA-)+c(H2A)=0.2molL-1
B.NaHA溶液的pH<7
C.曲线Ⅰ代表A2-,曲线Ⅲ代表H2A
D.V(盐酸)=30mL时,c(Na+)=2c(A2-)+2c(HA-)+2c(H2A)
【答案】B
【解析】
Na2A与盐酸反应:Na2A+HCl=NaHA+NaCl、NaHA+HCl=NaCl+H2A,根据反应过程以及图像,可以推出I代表A2-,II代表HA-,III代表的是H2A,据此分析;
Na2A与盐酸反应:Na2A+HCl=NaHA+NaCl、NaHA+HCl=NaCl+H2A,该图像是![]() 溶液中滴加盐酸,则由图可知,曲线Ⅰ是
溶液中滴加盐酸,则由图可知,曲线Ⅰ是![]() ,曲线Ⅱ是
,曲线Ⅱ是![]() ,曲线Ⅲ是
,曲线Ⅲ是![]() 。
。
A. 根据物料守恒,![]() 溶液中存在:
溶液中存在:![]() ,故A说法正确;
,故A说法正确;
B. ![]() 时,溶液中溶质为NaHA,
时,溶液中溶质为NaHA,![]() ,说明
,说明![]() 的水解程度大于其电离程度,此时溶液显碱性,
的水解程度大于其电离程度,此时溶液显碱性,![]() ,故B说法错误;
,故B说法错误;
C. 根据上述分析可知,曲线Ⅰ代表![]() ,曲线Ⅲ代表
,曲线Ⅲ代表![]() ,故C说法正确;
,故C说法正确;
D. 根据物料守恒,![]() ,故D说法正确。
,故D说法正确。
答案:B。

【题目】研究碳、氮及其化合物的转化对于环境的改善有重大意义。
(1)氧化还原法消除NOx的转化如下:NO![]() NO2
NO2![]() N2
N2
已知:NO(g)+O3(g)===NO2(g)+O2(g) ΔH=-200.9 kJ·mol-1
2NO(g)+O2(g)===2NO2(g) ΔH=-116.2 kJ·mol-1
则反应Ⅰ的热化学方程式为___________________________________________________________。
(2)有人设想将CO按下列反应除去:2CO(g)===2C(s)+O2(g) ΔH>0,请你分析该设想能否实现?________(填“能”或“否”),依据是_________________________________________。
(3)一定条件下,CO可与粉末状的氢氧化钠作用生成甲酸钠。已知常温时,甲酸的电离平衡常数Ka=1.70×10-4。
①甲酸钠的水溶液呈碱性,请用离子方程式表示其原因________________________________________。
②向20 mL 0.1 mol·L-1的甲酸钠溶液中滴加10 mL 0.1 mol·L-1的盐酸,混合液呈________(填“酸”或“碱”)性,溶液中离子浓度从大到小的顺序为_________________________________。
(4)活性炭也可用于处理汽车尾气中的NO。在2 L恒容密闭容器中加入0.100 0 mol NO和2.030mol固体活性炭,生成A、B两种气体,在不同温度下测得平衡体系中各物质的物质的量如表所示:
温度 | 固体活性炭/mol | NO/mol | A/mol | B/mol |
200 ℃ | 2.000 | 0.040 0 | 0.030 0 | 0.030 0 |
335 ℃ | 2.005 | 0.050 0 | 0.025 0 | 0.025 0 |
①该反应的正反应为________(填“吸热”或“放热”)反应。
②200 ℃时,平衡后向恒容容器中再充入0.1 mol NO,再次平衡后,NO的百分含量将________(填“增大”“减小”或“不变”)。
③计算反应在335 ℃时的平衡常数为________。



