题目内容
(本题共8分)
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示_________________,
K值大小与温度的关系是:温度升高,K值______________
(填一定增大、一定减小、或可能增大也可能减小)。
(2)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:
CO(g)十H2O(g) 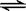 CO2(g)十H2 (g)十Q(Q>0)
CO2(g)十H2 (g)十Q(Q>0)
CO和H2O浓度变化如下图,则 0—4min的平均反应速率v(CO)=______ mol/(L·min)

(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3min—4min之间反应处于_________状态; C1数值_________0.08 mol/L (填大于、小于或等于)。
②反应在4min—5min问,平衡向逆方向移动,可能的原因是________(单选),表中5min—6min之间数值发生变化,可能的原因是__________(单选)。
a.增加水蒸气 b.降低温度
c.使用催化剂 d.增加氢气浓度
(1) 可逆反应的进行程度越大 可能增大也可能减小
(2) 0.03 (3) ①平衡 > ②d a
【解析】考查平衡常数计算和判断。
(1)平衡常数是指在一定条件下,可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,因此K值越大,表示可逆反应的进行程度越大。由于升高温度,平衡可能向正反应方向移动,也可能向逆反应方向移动,所以K值可能增大,也可能减小。
(2)根据图像可知,再 0—4min内CO的浓度减小了0.20mol/L-0.08mol/L=0.12mol/L,所以其反应速率是0.12mol/L÷4min=0.03mol/(L·min)。
(3)①根据表中数据可知,在此时间内,物质的浓度是不变的,所以反应处于平衡状态。由于反应是放热反应,所以升高温度,平衡向逆反应方向移动,因此CO的浓度大于0.08mol/L。
②增大反应物浓度合伙降低温度,平衡向正反应方向移动。而催化剂不能改变平衡状态。所以应该是增大了氢气浓度,平衡向逆反应方向移动,答案选d。根据表中数据可知,5min—6min是CO的浓度减小,而水蒸气和氢气的浓度增大,说明改变的条件是增大了水蒸气的浓度,平衡向正反应方向移动,答案选a。

 名校课堂系列答案
名校课堂系列答案(本题共8分)现有部分元素的性质与原子(或分子)结构如下表:
|
元素编号 |
元素性质与原子(或分子)结构 |
|
T |
最外层电子数是次外层电子数的3倍 |
|
X |
常温下单质为双原子分子,分子中含有3对共用电子对 |
|
Y |
M层比K层少1个电子 |
|
Z |
第三周期元素的简单离子中半径最小 |
(1)写出元素T的原子结构示意图 。
(2)元素Y与元素Z相比,金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是________(填序号)。
a.Y单质的熔点比Z单质低
b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈
d.Y最高价氧化物的水化物的碱性比Z强
(3)T、X、Y、Z中有两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的电子式:_____ _________。
(4)元素T和氢元素可形成一种18电子的化合物Q,元素X与氢元素也能按原子个数比为1∶2形成一种18电子化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式: 。
 CH3OH(g)+H2O(g)
+49.0 kJ。反应在2分钟时达到了平衡。
CH3OH(g)+H2O(g)
+49.0 kJ。反应在2分钟时达到了平衡。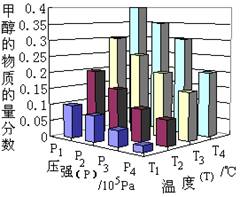
 2Na2SiO3+CaSiO3+3CO2↑
2Na2SiO3+CaSiO3+3CO2↑