题目内容
用NA表示阿伏加德罗常数,下列叙述正确的是
| A.标准状况下,22.40 L H2O含有的分子数为NA |
| B.常温常压下,1.06 gNa2CO3含有的Na+离子数为0.02NA |
| C.通常状况下,NA个CO2分子占有的体积为22.40L |
| D.物质的量浓度为0.50mol/L的MgCl2溶液中,含有C1-个数为NA |
B
解析试题分析:A选项,标况下,水是液态,无法根据体积求算物质的量;B选项, 1.06g Na2CO3晶体物质的量=C=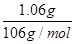 =0.01mol,含钠离子0.02mol,B正确;C选项,标准状况下,NA个CO2分子占有的体积为22.40L,C错误;D选项,物质的量浓度为0.50mol/L的MgCl2溶液中, C1-的物质的量浓度为1mol/L,不知道体积的前提下无法求出C1-的个数。
=0.01mol,含钠离子0.02mol,B正确;C选项,标准状况下,NA个CO2分子占有的体积为22.40L,C错误;D选项,物质的量浓度为0.50mol/L的MgCl2溶液中, C1-的物质的量浓度为1mol/L,不知道体积的前提下无法求出C1-的个数。
考点:物质的量的相关计算。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列各溶液中NO3-物质的量浓度最大的是
| A.20 mL 2 moL/L Mg(NO3)2 |
| B.100 mL 2.5 mot/L NaNO3 |
| C.25 mL 1.0mol/L Al(NO3)3 |
| D.30 mL 2.5 mol/L NH4NO3 |
将一定的 、
、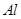 合金置于水中,结果合金完全溶解,得到20mL、PH=14的溶液,然后用1mol/L的盐酸滴定至沉淀最大时,消耗40mL盐酸。原合金中
合金置于水中,结果合金完全溶解,得到20mL、PH=14的溶液,然后用1mol/L的盐酸滴定至沉淀最大时,消耗40mL盐酸。原合金中 的物质的量( )
的物质的量( )
| A.0.01mol | B.0.02mol | C.0.03mol | D.0.04mol |
NA表示阿佛加德罗常数,下列说法正确的是
A.18gNH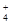 含有电子数为10NA 含有电子数为10NA |
| B.1mol任何气体的体积都约是22.4L |
| C.NA个H2SO4分子的质量等于H3PO4的摩尔质量 |
| D.标准状况下,相同体积的O2、HCl、H2O含有的分子数相同 |
已知3.01×1023个X气体分子的质量为16g,则X气体的摩尔质量是
| A.16g | B.32g | C.64g /mol | D.32g /mol |
用NA表示阿伏加德罗常数的值。下列判断错误的是
| A.足量Fe与1mol Cl2充分反应电子转移数为2NA |
| B.NA个H+的质量为1g |
| C.2 L 0.5mol/L Na2SO4溶液中含2NA个Na+ |
| D.标准状况下,22.4L水中含有NA个分子 |
现有装有物质的量浓度为1.2 mol/L的盐酸100ml的容器甲和装有物质的量浓度为1mol/L的硫酸100ml的容器乙,向甲.乙容器内加入相同质量的铝,充分反应后生成氢气的体积比为3:4(标准状况下),问所加入的铝的质量是( )
| A.1.08克 | B.1.44克 | C.1.8 克 | D.无法计算 |
乙烯的产量是衡量一个国家石油化工发展水平的重要标志。下列有关表述正确的是
A.乙烯的电子式是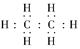 |
| B.乙烯的结构式为CH2CH2 |
C.乙烯中碳原子的结构示意图为 |
| D.5.6L乙烯中含有1mol C—H键 |
有以下四种物质:① 标况下11.2L CO2②1g H2③1.204×1024个N2 ④4℃时18 mLH2O,下列说法不正确的是: ( )
| A.分子个数:③>④>①=② | B.原子个数:③>④>①>② |
| C.体 积:③>④>①=② | D.质 量:③>①>④>② |