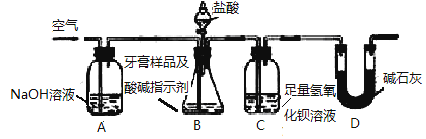
题目内容
【题目】(1)一定条件下,向容积为2L的恒容密闭容器中充入1 mol CH3OH(g)和3 mol H2O(g),CH3OH(g) + H2O(g)![]() CO2(g) + 3H2(g)
CO2(g) + 3H2(g) ![]() H(298K)=+ 49.4 kJ/mol。实验测得:达到平衡状态时,吸收热量19.76 kJ。则
H(298K)=+ 49.4 kJ/mol。实验测得:达到平衡状态时,吸收热量19.76 kJ。则
①达平衡时混合气体的压强是反应前的 倍。
②该条件下反应达平衡状态的依据是(填序号) 。
A.v正(CH3OH)=v正(CO2) B.混合气体的密度不变
C.c(CH3OH)=c(H2O) D.混合气体的总物质的量不变
(2)在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热Q kJ。则表示甲醇燃烧热的热化学方程式为_____________________。
(3)对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
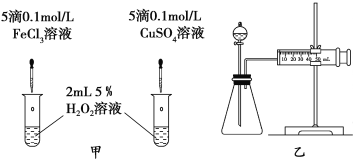
①定性分析:如图甲可通过观察__________________,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是______________。
②定量分析:用图乙所示装置做对照实验,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。检查该装置气密性的方法是 ,实验中需要测量的数据是_______________。
【答案】(1)①1.2②D(2)CH3OH(l)+3/2O2(g)![]() CO2(g)+2H2O(l)ΔH=-32QkJ·mol-1
CO2(g)+2H2O(l)ΔH=-32QkJ·mol-1
(3)①反应产生气泡的快慢;控制阳离子相同,排除阴离子的干扰;②关闭分液漏斗活塞,将注射器活塞向外拉出一定距离,一段时间后松开,观察活塞是否回到原位。收集40mL气体所需时间
【解析】
试题分析:CH3OH(g) + H2O(g)![]() CO2(g) + 3H2(g)---49.4 kJ ,放热19.76 kJ,消耗CH3OH 的量 X=0.4mol.,剩余各物质的量:甲醇0.6 mol, 水2.6 mol 二氧化碳0.4 mol 氢气1.2mol;气体的压强之比与气体的物质的量成正比:反应后:0.6+2.6+0.4+1.2=4.8 mol,反应前:1+3=4 mol,4.8/4=1.2;
CO2(g) + 3H2(g)---49.4 kJ ,放热19.76 kJ,消耗CH3OH 的量 X=0.4mol.,剩余各物质的量:甲醇0.6 mol, 水2.6 mol 二氧化碳0.4 mol 氢气1.2mol;气体的压强之比与气体的物质的量成正比:反应后:0.6+2.6+0.4+1.2=4.8 mol,反应前:1+3=4 mol,4.8/4=1.2;
(1)该条件下反应达平衡状态的依据是V 正=V逆,v正(CH3OH)=v正(CO2),同向,无法判断;容器的体积不变,反应前后气体的质量不变,密度为定值。无法判断;该反应为反应前后体积可变的反应,混合气体的总物质的量不变,反应达平衡状态。
(2)1 g CH3OH燃烧生成液态水时放热Q kJ。则1摩尔CH3OH燃烧生成液态水时放热32Q kJ则表示甲醇燃烧热的热化学方程式为CH3OH(l)+3/2O2(g)![]() CO2(g)+2H2O(l) ΔH=-32QkJ·mol-1;
CO2(g)+2H2O(l) ΔH=-32QkJ·mol-1;
(3)双氧水在催化剂作用下,分解产生氧气,因此可以观察反应产生气泡的快慢;为了便于比较催化效率,阳离子不同,阴离子一样,便于比较。
(4)检查该装置气密性的方法是:形成密闭体系,造成压强差;检验时均以生成40 mL气体为准,那么就测量收集40 mL气体所需要的时间长短。不同的催化剂催化能力不同,所需时间不同。

 名校课堂系列答案
名校课堂系列答案【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g) + Y(g)![]() 2Z(g) △H<0,一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H<0,一段时间后达到平衡,反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A. 0~2min的平均速率ν(Z) = 2.0×10-3mol·L-1·min-1
B. 其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正)
C. 该温度下此反应的平衡常数K =1.44
D. 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大