题目内容
【题目】假设图中原电池产生的电压、电流强度均能满足电解、电镀要求,即为理想化。①~⑧为各装置中的电极编号。当K闭合后,下列说法正确的有( )
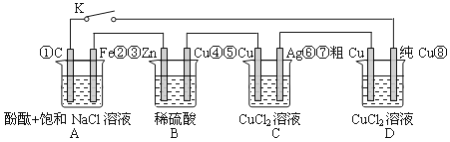
①D装置中纯Cu电极反应为:Cu2++2e-=Cu
②整个电路中电子的流动方向为:③→②;①→⑧;⑦→⑥;⑤→④;
③C装置原理上是一个电镀池(Ag表面镀Cu),期中Cu作阴极,Ag作阳极
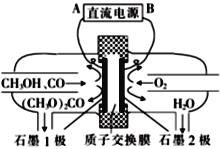
④A装置中C电极反应为:O2+4e-+2H2O=4OH-
A. ③④ B. ①② C. ②③④ D. ①②④
【答案】B
【解析】根据装置可判断,B装置是原电池,其中锌是负极,铜是正极,A、C、D是电解池。①D装置中纯Cu作阴极,粗铜作阳极,为铜的电解精炼装置,纯Cu电极反应为:Cu2++2e-=Cu,故①正确;②B装置中锌是负极,铜是正极,整个电路中电子的流动方向为:③→②;①→⑧;⑦→⑥;⑤→④,故②正确;③C装置中铜是阳极,银是阴极,为在银上镀铜的装置,故③错误;④当K闭合时,A装置中的铁与负极相连,做阴极,C为阳极,溶液中的氯离子放电生成氯气,故④错误;正确的有①②,故选B。

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
【题目】部分弱酸的电离平衡常数如表所示:
弱酸 | HCOOH | HCN | H2CO3 |
电离平衡常数(25℃) | K=1.77×10-4 | K=6.2×10-10 | K1=4.4×10-7 K2=4.7×10-11 |
下列选项错误的是( )
A. 2CN-+H2O+CO2===2HCN+CO![]()
B. 2HCOOH+CO![]() ===2HCOO-+H2O+CO2↑
===2HCOO-+H2O+CO2↑
C. 中和等体积,等pH的HCOOH和HCN消耗NaOH的量前者小于后者
D. 等体积等浓度的HCOONa和NaCN溶液中所含离子总数前者大于后者