题目内容
8.下列各组物质的分离或提纯,应选用下述方法的哪一种?(用编号填空)A、分液 B、过滤 C、萃取 D、蒸馏 E、蒸发结晶 F、加热分解
①除去Ca(OH)2溶液中悬浮的CaCO3B;
②从碘水中提取碘C;
③用自来水制取蒸馏水D;
④除去碳酸钠固体中少量的碳酸氢钠固体F;
⑤分离植物油和水A.
分析 ①碳酸钙不溶于水,而氢氧化钙溶于水;
②碘不易溶于水,易溶于有机溶剂;
③水的沸点较低;
④碳酸氢钠加热分解生成碳酸钠;
⑤植物油和水混合分层.
解答 解:①碳酸钙不溶于水,而氢氧化钙溶于水,则过滤可除杂,故答案为:B;
②碘不易溶于水,易溶于有机溶剂,则选择萃取从碘水中提取碘,故答案为:C;
③水的沸点较低,则选择蒸馏法用自来水制取蒸馏水,故答案为:D;
④碳酸氢钠加热分解生成碳酸钠,则加热分解除杂,故答案为:F;
⑤植物油和水混合分层,则选择分液法分离,故答案为:A.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及混合物分离提纯为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
18.对于可逆反应2SO2 (g)+O2(g)?2SO3(g)△H<0在一定温度下其平衡数为K,下列说法正确的是( )
| A. | 增大SO2的转化率K值一定增大 | B. | 减小压强K值减小 | ||
| C. | 升高温度K值增大 | D. | K值越大SO2转化率越大 |
19.下列反应中二氧化硫被氧化的是( )
| A. | SO2+2H2S═3S+2H2O | B. | SO2+2NaOH═Na2SO3+H2O | ||
| C. | SO2+H2O═H2SO3 | D. | SO2+Cl2+2H2O═4H++2Cl-+SO42- |
16.下列各组离子在给定条件下能大量共存的是( )
| A. | 能使酚酞试液变红的溶液中:Na+、Cl-、SO42-、Fe3+ | |
| B. | c(H+):c(OH-)=105:1的溶液中:K+、HCO3-、Cl-、Na+ | |
| C. | c(H+)=1.0×10-13mol•L-1的溶液中:Na+、SO42-、Al(OH)4-、CO32- | |
| D. | 强酸性溶液中:NH4+、I-、Fe2+、NO3- |
13.N、O、Na、Mg、S、Br是常见的六种元素.
(1)Br位于元素周期表第四周期第VIIA族;Na和O形成1:1的化合物的电子式: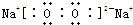 .该物质含有的化学键为:离子键和非极性键.
.该物质含有的化学键为:离子键和非极性键.
(2)用“>”或“<”填空:
(3)已知多硫化钠一溴储能电池是一种二次电池,结构如图.电池总反应为:2Na2S3+2NaBr$?_{放电}^{充电}$3Na2S2+Br2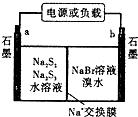
①放电时Na+向b极迁移(填“a或b,”).
②放电时负极的电极反应式为:3S22--2e-=2S32-
(4)已知N4为正四面体结构,N-N键能为167kJ•mol-1,N≡N键能为942kJ•mol-1.写出N4(g)转化为N2(g)的热化学方程式N4(g)=2N2(g)△H=-882kJ/mol.
(1)Br位于元素周期表第四周期第VIIA族;Na和O形成1:1的化合物的电子式:
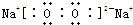 .该物质含有的化学键为:离子键和非极性键.
.该物质含有的化学键为:离子键和非极性键.(2)用“>”或“<”填空:
| 稳定性 | 粒子半径 | 熔点 | 键的极性 |
| NH3<H2O | O2-> Mg2+ | SO3< Na2O2 | H-O> H-N |

①放电时Na+向b极迁移(填“a或b,”).
②放电时负极的电极反应式为:3S22--2e-=2S32-
(4)已知N4为正四面体结构,N-N键能为167kJ•mol-1,N≡N键能为942kJ•mol-1.写出N4(g)转化为N2(g)的热化学方程式N4(g)=2N2(g)△H=-882kJ/mol.
20.下列实验操作的描述符合实验事实的是( )
| A. | 中和滴定实验中,滴定管和锥形瓶都要先洗涤、再润洗 | |
| B. | 用四氯化碳萃取碘水中的碘时,将碘的四氯化碳溶液从分液漏斗下口放出 | |
| C. | 分馏时,温度计的水银球插入液面以下 | |
| D. | 除去KNO3中的NaCl杂质,可用溶解→加AgNO3溶液→过滤方法 |
17.下列各金属作还原剂时,还原性最强的是( )
| A. | Al | B. | Fe | C. | Cu | D. | Na |
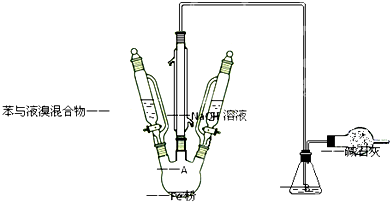
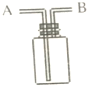 今有下列气体:H2、Cl2、O2、HCl、NH3、NO(难溶于水).用如图所示装置进行实验,请写下列空白:
今有下列气体:H2、Cl2、O2、HCl、NH3、NO(难溶于水).用如图所示装置进行实验,请写下列空白: