题目内容
(1)空气中的硫氧化物和氮氧化物随雨水降下就会形成酸雨,酸雨的主要成分是亚硫酸、硫酸和硝酸。试用化学方程式表示它们的形成过程:________________________,_____________________________,___________________________。(可不填满,也可补充)(2)某校化学兴趣小组对当地的一次雨水进行了pH测定。雨水刚降下时,pH为5.0;6小时后测量,pH为4.6,紧接着再次测量,pH仍为4.6。是他们的初次测量有误,还是雨水的pH果真发生了变化?请谈谈你的观点:___________________________。(可用化学语言表述)
解析:(1)空气的硫氧化物是二氧化硫和三氧化硫,空气中氮氧化物主要是二氧化氮,它们与水反应分别生成亚硫酸、硫酸和硝酸。同时也有一氧化氮被氧化为硝酸,一氧化氮主要是二氧化氮溶于水生成的。
(2)酸雨中溶有氧气,能将弱酸亚硫酸氧化为强酸硫酸(硝酸很稀,氧化性很弱,不能氧化亚硫酸),故而溶液的酸性增强,pH降低。
答案:(1)SO2+H2O![]() H2SO3 SO3+H2O
H2SO3 SO3+H2O![]() H2SO4 3NO2+H2O
H2SO4 3NO2+H2O![]() 2HNO3+NO(或4NO2+O2+2H2O
2HNO3+NO(或4NO2+O2+2H2O![]() 4HNO3) 4NO+3O2+2H2O
4HNO3) 4NO+3O2+2H2O![]() 4HNO3(不答亦可)
4HNO3(不答亦可)
(2)2H2SO3+O2![]() 2H2SO4
2H2SO4

练习册系列答案
相关题目
硫酸亚铁是一种可用于治疗缺铁性贫血的药剂.硫酸亚铁药片外表包有一层特制的糖衣,以保护硫酸亚铁不被空气中的氧气氧化成硫酸铁(硫酸铁无治疗贫血的药效).
(1)请完成硫酸亚铁在硫酸酸化的条件下与空气中的氧气反应的离子方程式:
Fe2+ O2+ H+-- Fe3++ H2O 反应中的氧化剂是 (填化学式).
(2)试设计一个实验方案,探究某硫酸亚铁药片是否被氧化.请在答题卡的表格中(可以不填满,表格不够时也可自行添加)写出实验步骤以及预期现象和结论.
限选实验试剂:0.1moL?L-1 KSCN、氯水.
(3)步骤2的离子方程式为 .
(1)请完成硫酸亚铁在硫酸酸化的条件下与空气中的氧气反应的离子方程式:
(2)试设计一个实验方案,探究某硫酸亚铁药片是否被氧化.请在答题卡的表格中(可以不填满,表格不够时也可自行添加)写出实验步骤以及预期现象和结论.
限选实验试剂:0.1moL?L-1 KSCN、氯水.
| 实验步骤 | 预期现象和结论 |
| 步骤1:把药品刮去糖衣,用研钵研碎;取少量研碎的粉末在试管中,用少量的蒸馏水溶解; | 硫酸亚铁在蒸馏水中溶解. |
| 步骤2: |
|
| 步骤3: |
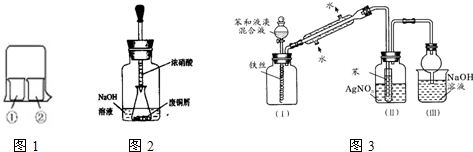
 (2013?菏泽二模)X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图1所示(水及部分产物已略去).
(2013?菏泽二模)X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图1所示(水及部分产物已略去).