题目内容
【题目】下列说法正确的是
A. 在实验室中可以用己烯通萃萃取提取溴水中的溴单质
B. 在一定条件下乙烯可被氧化成乙醇,乙醇可以被氯化为乙酸
C. lmol葡萄糖能水解生成2molCH3CH2OH和2molC02
D. 乙烯使酸性高锰酸钟溶液褪色与乙烯使漠水褪色的原理不同
【答案】D
【解析】A、己烯能与溴发生加成反应,选项A错误;B、在一定条件下乙烯与水发生加成反应生成乙醇,选项B错误;C、葡萄糖为单糖,不能水解,在无氧呼吸条件下,1mol葡萄糖可以生成2molCH3CH2OH和2molCO2,选项C错误;D、乙烯使酸性高锰酸钾溶液褪色是发生氧化反应,乙烯使溴水褪色是发生加成反应,原理不同,选项D正确。答案选D。

【题目】某实验小组用0.50mol/L NaOH溶液和0.50mol/L 硫酸溶液进行中和热的测定,实验装置如图所示。
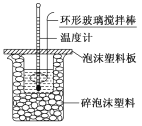
(1)已知中和热的理论值△H= -57.3kJ·mol-1,写出NaOH溶液和稀硫酸反应的中和热的热化学方程式:_______________。
(2)取50mLNaOH溶液和30mL硫酸溶液进行实验,实验数据如下表。
实验组 | 起始温度t1/℃ | 终止温度 t2/℃ | |
H2SO4 | NaOH | ||
1 | 26.2 | 26.0 | 30.1 |
2 | 27.0 | 27.4 | 33.1 |
3 | 26.4 | 26.2 | 30.5 |
①中和热△H=____________(取小数点后一位)。[已知:比热容c=4.18J·(g·℃)-1]
②上述实验数值结果与-57.3 kJ·mol-1有偏差,产生偏差的原因可能是______(填字母)。
a.实验装置保温、隔热效果差
b.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
c.量取NaOH溶液的体积时仰视读数
d.用温度计测定NaOH溶液起始温度后直接测量硫酸的温度
(3)若取100mL0.50mol/L NaOH溶液和50mL0.50mol/L 硫酸进行中和热的测定,其它实验条件相同,则所测得中和热的数值______(填“偏大”、“偏小”或“不变”)。
(4)已知一元弱酸HA(aq)与NaOH(aq)反应生成1mol H2O(l)时的△H= -23.1 kJ·mol-1,依据中和热的理论值,则HA(aq)![]() H+(aq)+A-(aq)的△H=____________。
H+(aq)+A-(aq)的△H=____________。
【题目】五氧化二钒广泛用于冶金、化工等行业,主要用于冶炼钒铁.用作合金添加剂,占五氧化二钒总消耗量的80%以上,其次是用作有机化工的催化剂,为了增加V2O5的利用率,我们从废钒催化剂(主要成分V2O5,VOSO4,K2SO4,SiO2和Fe2O3等)中回收V2O5的一种生产工艺流程示意图如下:
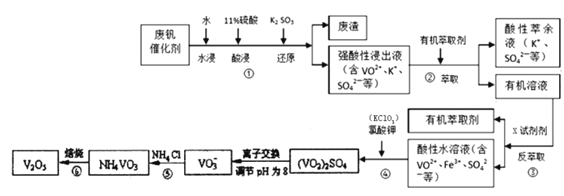
部分含钒物质在水中的溶解性如下,回答下列问题:
物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
溶解牲 | 可溶 | 难溶 | 难溶 | 易溶 |
(l)①中废渣的主要成分是____;①中V2O5发生反应的离子方程式为_____________。
(2)②,③中的变化过程可简化为(下式中的R表示VO2+或Fe3+,HA表示有机萃取剂的主要成分):R2(SO4)n(水层)+2nHA(有机层)![]() 2RA(有机层)+nH2SO4(水层)。②中萃取时必须加入适量碱,其原因是________________;实验室进行萃取操作主要使用的玻璃仪器为________________。
2RA(有机层)+nH2SO4(水层)。②中萃取时必须加入适量碱,其原因是________________;实验室进行萃取操作主要使用的玻璃仪器为________________。
(3)实验室用的原料中V2O5占6%(原料中的所有钒已换算成V2O5)。取l00g该废钒催化剂按工业生产的步骤进行实验,当加入100 mL0.1mol/L的KC1O3溶液时,溶液中的钒恰好被完全处理,假设以后各步钒没有损失,则该实验中钒的回收率是____(己知V2O5的相对分子质量为182)。
(4) 25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间的关系如下表:
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
钒沉淀率/% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.6 | 96.4 | 93.1 | 89.3 |
试判断在实际生产时,⑤中加入氨水调节溶液的最佳pH为_________;若钒沉淀率为93.1%时不产生Fe( OH)3沉淀,则此时溶液中c(Fe3+)=_________。(已知:25℃时k[Fe(OH)3]=2.6×l0-39.)