题目内容
气态氯化铝(Al2Cl6)是具有配位键的化合物,分子中原子间成键的关系如图所示.若将图中是配位键的斜线上加上箭头,下列4个选项中正确的是( )
A、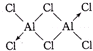 |
B、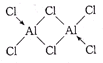 |
C、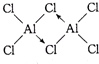 |
D、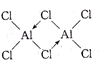 |
考点:配合物的成键情况
专题:化学键与晶体结构
分析:先分析铝原子和氯原子的最外层电子,再根据每个原子达到8电子稳定结构分析配位键成键情况.
解答:
解:Cl原子最外层有7个电子,只能与Al原子各提供1个电子形成一个共价键,使自己达到8电子稳定结构.Al原子最外层有3个电子,可分别与3个Cl原子形成共价键,因而Cl原子与2个Al原子形成的化学键中,必有1个是配位键,由于电子对由Cl原子提供,这样Cl原子最外层电子数仍为8,Al原子最外层也成为8电子结构.
故选D.
故选D.
点评:本题考查了配位键的成键情况,配位键成键时必须有提供空的轨道的原子、有提供孤对电子的原子,且配位键由提供孤对电子的原子指向提供空轨道的原子,配位键也属化学键.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案
相关题目
下列烃中,苯环上的一氯代物的同分异构体数目最少的是( )
| A、邻二甲苯 | B、间二甲苯 |
| C、对二甲苯 | D、乙苯 |
设NA表示表示阿伏伽德罗常数,下列叙述正确的是( )
| A、1mol NH4+含有的电子数为1NA |
| B、标况下22.4L Cl2溶于水,转移电子数为1NA |
| C、0.1L 3mol/L的NH4NO3溶液中氮原子数等于0.6NA |
| D、3mol NO2溶于水转移电子3mol |
下列烃中,一卤代物的同分异构体的数目最多的是( )
| A、乙烷 |
| B、2-甲基丙烷 |
| C、2,2-二甲基丙烷 |
| D、2,2,3,3-四甲基丁烷 |
下列变化中,属于化学变化的是( )
| A、用苯从溴水中萃取溴 |
| B、重油裂化得到轻质燃料油 |
| C、从煤焦油中提取苯、甲苯、二甲苯 |
| D、石油分馏得到汽油、煤油等产物 |
已知在25℃、101kPa下,1g C8H18(辛烷)燃烧生成二氧化碳和液态水放出48.40kJ热量,表示上述反应的热化学方程式正确的是( )
| A、C8H18(l)+O2(g)═8CO2(g)+9H2O△H=-48.40 kJ?mol-1 |
| B、C8H18(l)+O2(g)═8CO2(g)+9H2O(l)△H=-5 518 kJ?mol-1 |
| C、C8H18(l)+O2(g)═8CO2(g)+9H2O(l)△H=+5 518 kJ?mol-1 |
| D、C8H18(l)+O2(g)═8CO2(g)+9H2O(l)△H=+48.40 kJ?mol-1 |
下列说法正确的是( )
| A、酸性氧化物都是非金属氧化物 |
| B、单质硅用来制作光导纤维 |
| C、水玻璃、漂白粉、胆矾、胶体属于混合物 |
| D、SO2能使氯水、品红溶液褪色、其原理不同 |
 据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示.下列说法正确的是( )
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示.下列说法正确的是( )| A、电池放电时Na+从b极区移向a极区 |
| B、电极b采用MnO2,MnO2既作电极材料又有催化作用 |
| C、该电池的负极反应为:BH4-+8OH-+8e-→BO2-+6H2O |
| D、每消耗3mol H2O2,转移的电子为3mol |
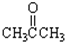 ;③CH3CH2Br;④
;③CH3CH2Br;④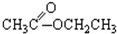 ;⑤
;⑤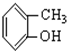 ;⑥
;⑥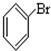 ;⑦
;⑦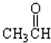 ;⑧
;⑧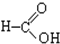 ;⑨
;⑨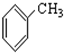 ;⑩
;⑩