题目内容
设NA表示表示阿伏伽德罗常数,下列叙述正确的是( )
| A、1mol NH4+含有的电子数为1NA |
| B、标况下22.4L Cl2溶于水,转移电子数为1NA |
| C、0.1L 3mol/L的NH4NO3溶液中氮原子数等于0.6NA |
| D、3mol NO2溶于水转移电子3mol |
考点:阿伏加德罗常数
专题:
分析:A.铵根离子中含有10个电子,1mol铵根离子含有10mol电子;
B.氯气溶于水,只有少量的氯气与水反应生成氯化氢和次氯酸;
C.1mol硝酸铵中含有2mol氮原子,根据n=cV计算出硝酸铵的物质的量及含有的氮原子数目.
D.二氧化氮与水反应生成硝酸和一氧化氮气体,3mol二氧化氮与水反应生成2mol硝酸,转移了2mol电子.
B.氯气溶于水,只有少量的氯气与水反应生成氯化氢和次氯酸;
C.1mol硝酸铵中含有2mol氮原子,根据n=cV计算出硝酸铵的物质的量及含有的氮原子数目.
D.二氧化氮与水反应生成硝酸和一氧化氮气体,3mol二氧化氮与水反应生成2mol硝酸,转移了2mol电子.
解答:
解:A.1mol铵根离子中含有10mol电子,含有的电子数为10NA,故A错误;
B.标况下22.4L氯气的物质的量为1mol,1mol氯气溶于水只有少量氯气与水反应生成氯化氢和次氯酸,反应转移的电子小于1mol,转移电子数小于1NA,故B错误;
C.0.1L 3mol/L的NH4NO3溶液中含有0.3mol硝酸铵,0.3mol硝酸铵中含有0.6mol氮原子,溶液中氮原子数等于0.6NA,故C正确;
D.3mol二氧化氮与水反应生成2mol硝酸和1mol一氧化氮,转移了2mol电子,故D错误;
故选C.
B.标况下22.4L氯气的物质的量为1mol,1mol氯气溶于水只有少量氯气与水反应生成氯化氢和次氯酸,反应转移的电子小于1mol,转移电子数小于1NA,故B错误;
C.0.1L 3mol/L的NH4NO3溶液中含有0.3mol硝酸铵,0.3mol硝酸铵中含有0.6mol氮原子,溶液中氮原子数等于0.6NA,故C正确;
D.3mol二氧化氮与水反应生成2mol硝酸和1mol一氧化氮,转移了2mol电子,故D错误;
故选C.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项C为易错点,转移硝酸铵中铵根离子和硝酸根离子中都含有氮原子,试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
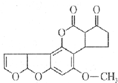 前不久,各大媒体在显著的位置刊登了关于900t致癌大米的报道,主要是变质大米中存在的黄曲霉素使人体中的特殊基因发生突变,有转变成肝癌的可能性.它的结构如图所示,和l mol该化合物起反应的H2或NaOH的最大值分别是( )
前不久,各大媒体在显著的位置刊登了关于900t致癌大米的报道,主要是变质大米中存在的黄曲霉素使人体中的特殊基因发生突变,有转变成肝癌的可能性.它的结构如图所示,和l mol该化合物起反应的H2或NaOH的最大值分别是( )| A、5mol,2mol |
| B、7mol,2mol |
| C、6mol,1mol |
| D、7mol,1mol |
下列关于粒子结构的描述不正确的是( )
| A、NF3和BF3是中心原子杂化类型相同的极性分子 |
| B、CH2Cl2和C2H4是空间构型不同的非极性分子 |
| C、在SiO2晶体中,Si原子与Si-O键数目比为1:2 |
| D、CF4和CO2是含极性键的非极性分子 |
溴水中存在着如下的平衡:Br2+H2O?HBr+HBrO,下列措施,不能使溶液颜色变浅的是( )
| A、通入乙烯气体 |
| B、通入SO2气体 |
| C、加入NaF晶体 |
| D、加入NaI晶体 |
在密闭容器中一定量混合气体发生反应:2A(g)+B(g)?xC(g),达到平衡时测得 A的浓度为 0.5mol/L,在温度不变的条件下,将容器的容积扩大到原来的2倍,再达平衡时测得A的浓度为 0.3mol/L,下列有关判断正确的是( )
| A、x=3 |
| B、平衡向正反应方向移动 |
| C、B的转化率降低 |
| D、C的体积分数增大 |
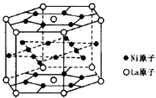 氢气是重要而洁净的能源,要利用氢气作能源,必须安全有效地储存氢气.有报道称某种合金材料有较大的储氢容量,其晶体结构的最小单元如图所示,则这种合金的化学式为( )
氢气是重要而洁净的能源,要利用氢气作能源,必须安全有效地储存氢气.有报道称某种合金材料有较大的储氢容量,其晶体结构的最小单元如图所示,则这种合金的化学式为( )| A、LaNi6 |
| B、LaNi3 |
| C、LaNi4 |
| D、LaNi5 |
以下物质不能由两种单质直接反应得到的是( )
| A、MgO |
| B、Na202 |
| C、S02 |
| D、S03 |