题目内容
16.设NA表示阿佛加德罗常数的值,下列说法不正确的是( )| A. | 1molD(氘)的质量与NA个T(氚)的质量相等 | |
| B. | NA个氧分子和NA个氢分子的质量比为16:1 | |
| C. | 28g氮气所含原子数目为2NA | |
| D. | 在标准状况下,0.5NA个氯气分子所占的体积约是11.2L |
分析 A、当物质的量相等时,物质的质量之比等于两物质的摩尔质量之比;
B、当物质的量相等时,物质的质量之比等于两物质的摩尔质量之比;
C、求出氮气的物质的量,然后根据1mol氮气含2mol氮原子来分析;
D、求出氯气的物质的量,然后根据V=nVm来计算.
解答 解:A、NA个T(氚)的物质的量为1mol,而当物质的量相等时,物质的质量之比等于两物质的摩尔质量之比,故1molD(氘)的质量与NA个T(氚)的质量之比等于两者的摩尔质量之比,即2:3,故A错误;
B、NA个氧气分子和NA个氢气分子的物质的量均为1mol,当物质的量相等时,物质的质量之比等于两物质的摩尔质量之比,即两者的质量之比为32:2=16:1,故B正确;
C、28g氮气的物质的量为1mol,而1mol氮气含2mol氮原子,即2NA个,故C正确;
D、0.5NA个氯气分子的物质的量为0.5mol,在标况下的体积V=nVm=0.5mol×22.4L/mol=11.2L,故D正确.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
6.室温下,向a mol/L氨水中逐滴加入盐酸,下列描述不正确的是( )
| A. | pH减小 | B. | $\frac{c(N{H}_{4}^{+})}{c(O{H}^{-})}$增大 | ||
| C. | 水的电离程度先减小后增大 | D. | Kb(NH3•H2O)不变 |
11.有机物X的分子式为C5H11Cl,用NaOH的醇溶液处理X,可得到分子式为C5H10的两种产物Y、Z.Y、Z经催化加氢后都可得到2-甲基丁烷.则X的结构简式可能为( )
| A. | CH3CH2CH2CH2CH2Cl | B. | 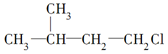 | ||
| C. |  | D. |  |
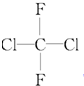
1.下列化学用语正确的是( )
| A. | 聚乙烯的结构简式: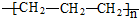 | B. | 丙烷分子的比例模型: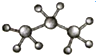 | ||
| C. | 四氯化碳分子的电子式: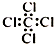 | D. | 2-乙基-1,3-丁二烯分子的键线式: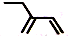 |
6.X、Y、Z、W四种金属片在稀盐酸中,用导线连接,可以组成原电池,实验结果如图所示:则四种金属的活泼性由强到弱的顺序为( )
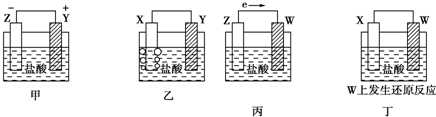

| A. | Z>Y>X>W | B. | Z>X>Y>W | C. | Z>Y>W>X | D. | Y>Z>X>W |
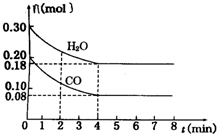 在一体积为2L的容器中,通入一定量的CO和H2O,850℃时发生反应:CO(g)+H2O(g)═CO2(g)+H2(g)
在一体积为2L的容器中,通入一定量的CO和H2O,850℃时发生反应:CO(g)+H2O(g)═CO2(g)+H2(g)
 和
和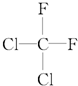
 和
和