题目内容
【题目】某研究小组利用如图装置探究SO2和Fe(NO3)3溶液的反应原理。回答下列问题:

(1)在实验室中,欲配制250g70%的浓硫酸,需要的玻璃仪器除量筒、烧杯外,还需要有__________,装置A中盛放浓硫酸的仪器名称是___________。
(2)往三颈烧瓶中通入N2的操作在滴加浓硫酸(填“之前”或“之后”),其目的是______________。
(3)三颈烧瓶中发生反应的化学方程式为_____________________,该反应中浓硫酸表现出的性质为______________。
(4)SO2易溶于水,下列装置可用于C处虚线框内吸收尾气的是___________(填编号)。
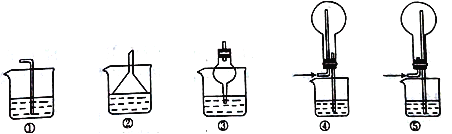
(5)装置B中产生白色沉淀的原因有两种可能。若要证明Fe3+能氧化SO2,则需要改进的地方是___________________,改进后若得到肯定结论,则装置B中发生反应的离子方程式为___________________、____________________。
【答案】 玻璃棒、分液漏斗 之前 排除装置内的空气,防止氧气对实验的干扰 Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O 强酸性 ②③④ 将装置B中的 硝酸铁溶液换成氯化铁溶液 SO2+2Fe3++2H2O=2Fe2++SO42-+4H+ SO42-+Ba2+=BaSO4↓
【解析】本题考查实验方案设计与评价,(1)配制一定质量分数的溶液,需要的仪器是烧杯、量筒、玻璃棒,因此缺少的仪器是玻璃棒;盛放浓硫酸的仪器是分液漏斗;(2)装置中有空气,可能氧气参与反应,干扰实验,因此先通一段时间的氮气,排除装置中的空气,然后再滴加浓硫酸;(3)三颈烧瓶中发生的反应是Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O,没有化合价的变化,因此体现浓硫酸的酸性;(4)SO2易溶于水,尾气处理需要防止倒吸,①装置不能防止倒吸,⑤装置进气管较短,容易引起倒吸,因此能防止倒吸的装置是②③④;(5)SO2溶于水,形成H2SO3,溶液显酸性,NO3-在酸性条件下具有强氧化性,容易把S元素氧化成SO42-,对实验产生干扰,因此用FeCl3替换Fe(NO3)3,离子反应方程式为:SO2+2Fe3++2H2O=2Fe2++SO42-+4H+ 、Ba2++SO42-=BaSO4↓。

 阅读快车系列答案
阅读快车系列答案【题目】向盛有H2O2溶液的试管中滴入少量浓盐酸,经检验生成的混合气体中只含有O2、Cl2、HCl和水蒸气。将气体通入X溶液(如图),依据观察到的现象,能判断气体中含有Cl2的是
选项 | X溶液 | 现象 |
|
A | 稀HNO3酸化的AgNO3溶液 | 有白色沉淀生成 | |
B | 滴有KSCN的FeSO4溶液 | 溶液变为血红色 | |
C | 淀粉KI酸性溶液 | 溶液变为蓝色 | |
D | 紫色石蕊溶液 | 溶液先变红后褪色 |
A. A B. B C. C D. D
【题目】在3个2 L的密闭容器中,在相同的温度下、使用相同的催化剂分别进行反应:
3H2(g)+N2(g) ![]() 2NH3(g)。按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下表。下列叙述正确的是
2NH3(g)。按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下表。下列叙述正确的是
容器编号 | 起始反应物 | 达到平衡的时间(min) | 平衡时N2的浓度(mol/L) | 平衡时气体密度 |
甲 | 3molH2、2molN2 | t1 | c1 | ρ1 |
乙 | 6molH2、4molN2 | 5 | 1.5 | ρ2 |
丙 | 2molNH3 | 8 | c3 | ρ3 |
A. 2ρ1=ρ2>ρ3
B. 容器乙中反应从开始到达平衡的反应速率为v(H2)=0.05mol/(L·min)
C. c1<c3
D. 2c1<1.5