题目内容
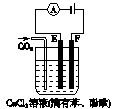
某同学用碳棒、铜棒和稀硫酸为原材料,实现了在通常条件下不能发生的反应:Cu+H2SO4(稀)====CuSO4+H2↑。
(1)请在方框内画出能够实现这一反应的实验装置图。
(2)某同学在做铜与稀硫酸的上述反应实验时,看到碳棒和铜棒都有气泡产生,但铜棒没有被腐蚀。请你分析其原因___________________,此时的电池反应为____________________。
(1)请在方框内画出能够实现这一反应的实验装置图。
| |
(1)
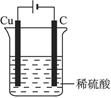
(2)电源反接 2H2O 2H2↑+O2↑
2H2↑+O2↑

(2)电源反接 2H2O
 2H2↑+O2↑
2H2↑+O2↑金属Cu活泼性排在氢的后面,所以不能是原电池,借助电解利用氧化还原反应设计成电解池,Cu为电解池的阳极,稀硫酸为电解液,C棒为电解池的阴极。

练习册系列答案
相关题目