题目内容
17.甲烷的分子组成相当于1个碳原子和2个氢分子,1mol甲烷在空气中充分燃烧 释放的热量与1mol碳和2mol氢气在空气中充分燃烧放热总量的关系是( )| A. | 前者大于后者 | B. | 前者小于后者 | ||
| C. | 两者相等 | D. | 没有相关燃烧热数据,无法对比 |
分析 甲烷在高温下分解可生成碳和氢气,1mol甲烷燃烧的产物与1mol碳和2mol氢气燃烧的产物相同,以此解答该题.
解答 解:1mol甲烷燃烧的产物与1mol碳和2mol氢气燃烧的产物相同,但甲烷在高温下发生分解反应生成碳和氢气,为吸热反应,可知1mol碳和2mol氢气在空气中充分燃烧放出的热量较多,
故选B.
点评 本题考查反应热与焓变的问题,为高频考点,侧重考查学生的分析能力和计算能力,本题注意把握甲烷的性质,从盖斯定律的角度思考,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.如图是滴定管和量筒的两个液面.下列有关读数中正确的是( )
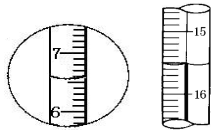

| A. | 左边是量筒读数6.5mL,右边是滴定管读数16.50mL | |
| B. | 左边是量筒读数7.5mL,右边是滴定管读数16.50mL | |
| C. | 左边是量筒读数6.5mL,右边是滴定管读数15.50mL | |
| D. | 左边是量简读数6.5mL,右边是滴定管读数16.50mL |
8.金属钒主要用于冶炼特种钢和在化学工业、炼油工业中作催化剂,被誉为“合金的维生素”.回收利用废钒催化剂(主要成分为V2O5、VOSO4和二氧化硅)的工艺流程如图所示.

(1)粉碎的作用是提高VOSO4(可溶性钒化合物)的浸出率,滤渣可用于制作光导纤维、建筑材料等(填用途).
(2)25时,取样进行实验分析,得到钒沉淀率和溶液pH之间的关系如表所示:
根据表数据判断,加入氨水调节溶液pH的最佳选择为1.7-1.8;上述过滤操作过程中所需用到的玻璃仪器有漏斗、烧杯、玻璃棒.
(3)为了提高钒的浸出率,用酸浸使废钒催化剂中的V2O5转变成可溶于水的VOSO4,酸浸过程中还原产物和氧化产物的物质的量之比为2:1.
(4)完成并配平氧化过程中的离子方程式:
1ClO3-+6VO2++6H+=6VO3++1Cl-+3H2O.
(5)废钒催化剂中V2O5的质量分数为6%(原料中的所有钒已换算成V2O5).取100g此废钒催化剂按上述流程进行实验,当加入105mL 0.1mol•L-1的KClO3溶液时,溶液中的钒恰好被完全处理,假设以后各步钒没有损失,则该工业生产中钒的回收率是95.55%.

(1)粉碎的作用是提高VOSO4(可溶性钒化合物)的浸出率,滤渣可用于制作光导纤维、建筑材料等(填用途).
(2)25时,取样进行实验分析,得到钒沉淀率和溶液pH之间的关系如表所示:
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率/% | 88.1 | 91.8 | 96.5 | 98 | 99.8 | 9.8 | 96.4 | 93.0 | 89.3 |
(3)为了提高钒的浸出率,用酸浸使废钒催化剂中的V2O5转变成可溶于水的VOSO4,酸浸过程中还原产物和氧化产物的物质的量之比为2:1.
(4)完成并配平氧化过程中的离子方程式:
1ClO3-+6VO2++6H+=6VO3++1Cl-+3H2O.
(5)废钒催化剂中V2O5的质量分数为6%(原料中的所有钒已换算成V2O5).取100g此废钒催化剂按上述流程进行实验,当加入105mL 0.1mol•L-1的KClO3溶液时,溶液中的钒恰好被完全处理,假设以后各步钒没有损失,则该工业生产中钒的回收率是95.55%.
12.同温同压下,等体积的两容器内分别充满NO和CO气体,下列对两容器中气体的判断正确的是( )
| A. | 分子数不同 | B. | 质子数相同 | C. | 氧原子数相同 | D. | 气体质量相同 |
2.某研究性小组用含铬废水制取具有强氧化性的重铬酸钾(K2Cr2O7),实验方案如图:
已知:
①Cr2O72-(橙色)+H2O?2CrO42-(黄色)+2H+
②金属离子沉淀的PH如表一:
表一:
③不同温度下化合物的溶解度如表二:
表二:
请回答:
(1)操作A的名称是抽滤(或过滤),加入硫酸的目的是将K2CrO4转化为K2Cr2O7.
(2)写出固体1中加入H2O2和KOH溶液后发生反应的离子方程式2Cr(OH)3+3H2O2+4OH-=2CrO42-+8H2O.
(3)操作B由多步组成,获得K2Cr2O7晶体的操作依次是:蒸发浓缩、操作1、洗涤1、操作2、抽滤、洗涤2、干燥.则下列说法正确的是AC.
A.操作1和操作2分别是趁热过滤和冷却结晶
B.洗涤1和洗涤2所用的洗涤剂分别为0℃的冷水和80℃的热水
C.当溶液出现过饱和现象时,振荡容器或用玻璃棒轻轻摩擦器壁均可促使晶体析出
D.进行洗涤2操作时,可开大水龙头,使洗涤剂快速通过沉淀物有利于将杂质洗尽
(4)为测定产品的纯度,可用摩尔盐[(NH4)2SO4•FeSO4•6H2O]标准溶液滴定,反应的离子方程式:
Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O
①请简述将已用移液管吸取的待测液转移至锥形瓶中的操作将移液管垂直放入稍倾斜的锥形瓶中,并使管尖与容器内壁接触,松开食指使溶液全部流出,数秒后,取出移液管.
②滴定时,先称取0.5000g K2Cr2O7 产品,溶于水配成100mL溶液,用0.1000mol/L的摩尔盐标准溶液进行滴定,数据记录如表三:
表三:
则测得K2Cr2O7产品的纯度是98%(以质量分数表示).
已知:

①Cr2O72-(橙色)+H2O?2CrO42-(黄色)+2H+
②金属离子沉淀的PH如表一:
表一:
| 离子 | 开始沉淀的PH | 沉淀完全的PH |
| Cr3+ | 4.9 | 6.8 |
| Fe3+ | 1.5 | 4.1 |
表二:
| 物质 | 溶解度/(g/110g水) | ||
| 0℃ | 40℃ | 80℃ | |
| K2SO4 | 7.4 | 14.8 | 21.4 |
| K2Cr2O7 | 4.7 | 26.3 | 73 |
(1)操作A的名称是抽滤(或过滤),加入硫酸的目的是将K2CrO4转化为K2Cr2O7.
(2)写出固体1中加入H2O2和KOH溶液后发生反应的离子方程式2Cr(OH)3+3H2O2+4OH-=2CrO42-+8H2O.
(3)操作B由多步组成,获得K2Cr2O7晶体的操作依次是:蒸发浓缩、操作1、洗涤1、操作2、抽滤、洗涤2、干燥.则下列说法正确的是AC.
A.操作1和操作2分别是趁热过滤和冷却结晶
B.洗涤1和洗涤2所用的洗涤剂分别为0℃的冷水和80℃的热水
C.当溶液出现过饱和现象时,振荡容器或用玻璃棒轻轻摩擦器壁均可促使晶体析出
D.进行洗涤2操作时,可开大水龙头,使洗涤剂快速通过沉淀物有利于将杂质洗尽
(4)为测定产品的纯度,可用摩尔盐[(NH4)2SO4•FeSO4•6H2O]标准溶液滴定,反应的离子方程式:
Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O
①请简述将已用移液管吸取的待测液转移至锥形瓶中的操作将移液管垂直放入稍倾斜的锥形瓶中,并使管尖与容器内壁接触,松开食指使溶液全部流出,数秒后,取出移液管.
②滴定时,先称取0.5000g K2Cr2O7 产品,溶于水配成100mL溶液,用0.1000mol/L的摩尔盐标准溶液进行滴定,数据记录如表三:
表三:
| 实验序号 | 待测样品溶液的体积/mL | 0.1000mol/L摩尔盐溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 0.00 | 24.98 |
| 2 | 25.00 | 1.56 | 29.30 |
| 3 | 25.00 | 1.00 | 26.02 |
9.A元素原子的核电荷数为11,B元素的质子数为8,A和B化合形成化合物Z,下列说法中错误的是( )
| A. | A可以形成+1价阳离子 | B. | B的最高价为+6价 | ||
| C. | Z一定可以与水反应 | D. | Z中不可能含有共价键 |
6.利用废碱渣(主要成分是Na2CO3)处理硫酸厂尾气中的SO2可制得无水Na2SO3(成品),其流程如图1:

(1)若欲利用废碱渣充分吸收SO2,则“吸收塔”内发生的主要反应的离子方程式为CO32-+2SO2+H2O═CO2+2HSO3-.
(2)处理过程中,要通过检验“吸收塔”排放出的尾气是否含有SO2来确定其是否达标.实验室中欲模拟检验尾气中的SO2,可以选用的试剂有bd;
a.澄清石灰水 b.硝酸酸化的Ba(NO3)2溶液 c.盐酸酸化的BaCl2溶液 d.品红溶液
(3)常温下,向“中和器”中加入适量NaOH后,溶液呈中性,则溶液中c(SO32-):c(HSO3-)=0.63[已知:常温下,Ka1(H2SO3)=l.5×10-2,Ka2(H2SO3)=6.3×10-8];
(4)图2所示为亚硫酸钠的溶解度曲线,则上述流程中的“结晶”方法是蒸发结晶(填“蒸发结晶”或“降温结晶”),图中a点所示分散系类别为浊液;
(5)仅用BaCl2和H2O2的混合溶液难以检出“成品“中的SO32-,原因是“成品”中含有某种杂质阴离子,该杂质阴离子SO42-(填化学式);实验室中常用如下方法检验SO32-:

己知25℃时,部分钡盐的Ksp数值如表:
若“溶液A”中SO32-浓度为0.01mol•L-1,且为杂质阴离子浓度的10倍,则向其中加入等体积0.01mol•L-1BaCl2溶液充分反应后c(Ba2+)=7×10-4mol•L-1,向“溶液B”中滴入BaCl2和H2O2的混合溶液时,发生反应的离子方程式为Ba2++H2O2+HSO3-═BaSO4↓+H++H2O.

(1)若欲利用废碱渣充分吸收SO2,则“吸收塔”内发生的主要反应的离子方程式为CO32-+2SO2+H2O═CO2+2HSO3-.
(2)处理过程中,要通过检验“吸收塔”排放出的尾气是否含有SO2来确定其是否达标.实验室中欲模拟检验尾气中的SO2,可以选用的试剂有bd;
a.澄清石灰水 b.硝酸酸化的Ba(NO3)2溶液 c.盐酸酸化的BaCl2溶液 d.品红溶液
(3)常温下,向“中和器”中加入适量NaOH后,溶液呈中性,则溶液中c(SO32-):c(HSO3-)=0.63[已知:常温下,Ka1(H2SO3)=l.5×10-2,Ka2(H2SO3)=6.3×10-8];
(4)图2所示为亚硫酸钠的溶解度曲线,则上述流程中的“结晶”方法是蒸发结晶(填“蒸发结晶”或“降温结晶”),图中a点所示分散系类别为浊液;
(5)仅用BaCl2和H2O2的混合溶液难以检出“成品“中的SO32-,原因是“成品”中含有某种杂质阴离子,该杂质阴离子SO42-(填化学式);实验室中常用如下方法检验SO32-:

己知25℃时,部分钡盐的Ksp数值如表:
| BaCO3 | BaSO4 | BaSO3 | BaS2O3 |
| 5.1×10-9 | 1.1×10-10 | 8.4×10-7 | 1.6×10-5 |
7. 某温度下,在2L密闭容器中发生反应:3A(g)+bB (g)?4C(g)△H=-Q kJ•mol-1(Q>0).12s 时达到平衡,反应物的物质的量的浓度(c)随时间(t)的变化如图所示.下列说法正确的是( )
某温度下,在2L密闭容器中发生反应:3A(g)+bB (g)?4C(g)△H=-Q kJ•mol-1(Q>0).12s 时达到平衡,反应物的物质的量的浓度(c)随时间(t)的变化如图所示.下列说法正确的是( )
 某温度下,在2L密闭容器中发生反应:3A(g)+bB (g)?4C(g)△H=-Q kJ•mol-1(Q>0).12s 时达到平衡,反应物的物质的量的浓度(c)随时间(t)的变化如图所示.下列说法正确的是( )
某温度下,在2L密闭容器中发生反应:3A(g)+bB (g)?4C(g)△H=-Q kJ•mol-1(Q>0).12s 时达到平衡,反应物的物质的量的浓度(c)随时间(t)的变化如图所示.下列说法正确的是( )| A. | 12s内,A的平均反应速率为0.025mol•L-1•s-1 | |
| B. | A的消耗反应速率等于B的消耗反应速率 | |
| C. | 第12s后,平衡体系的温度逐渐下降 | |
| D. | 12s内,A和B反应放出的热量为0.4Q kJ |