题目内容
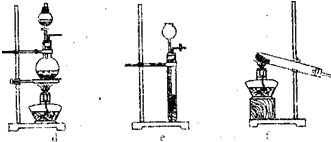
某研究小组进行与NH3有关的系列实验。(1)从图1-5-15中挑选所需的仪器,画出制取干燥NH3的装置简图(添加必要的塞子、玻璃导管、胶皮管。固定装置和尾气处理装置不用画),并标明所用试剂。
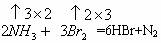
图1-5-15
(2)将NH3通入溴水中,有N2生成,反应的化学方程式为__________________。
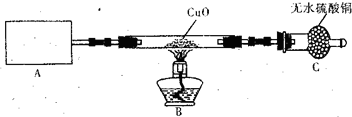
(3)为验证:“同温同压下,相同体积的任何气体都含有相同的数目的分子”,该小组同学设计了如下图1-5-16所示的装置,图中B管的容积是A管的2倍。活塞K1、K2、K3、K4、K5均关闭(固定装置和尾气处理装置略;HCl和NH3均不溶于石蜡油,也不与之反应;装置气密性好)。
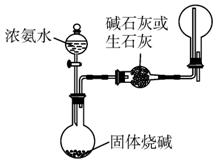
图1-5-16
①在A管中充满与大气压强相等的干燥HCl气体。操作是__________________。控制活塞K4、K5,调节C,使B管充满与A管同压的干燥NH3。
②缓慢开启活塞K3,A管中的现象是__________________。要达到实验目的,当反应完成并恢复到室温时,B管中预期的现象是__________;若观察不到预期现象,主要原因是_____________________________________________________________________。
解析:本题综合考查有关仪器的选择、组装、相关实验现象的描述与分析等内容。
(1)仔细观察所给仪器不难发现,没有给出酒精灯。则不能利用反应2NH4Cl+Ca(OH)2![]()
CuCl2+2NH3↑+2H2O来制备NH3,根据所给仪器的特点,结合NH3+H2O![]() NH3·H2O
NH3·H2O
![]()
![]() +OH-,不难对本题作答。
+OH-,不难对本题作答。
(2)NH3![]() N2化合价升高,Br2在化学反应中必定化合价降低,生成Br-,根据氧化还原方程式的配平方法,不难写出下列化学反应方程式:
N2化合价升高,Br2在化学反应中必定化合价降低,生成Br-,根据氧化还原方程式的配平方法,不难写出下列化学反应方程式:
![]() ,当NH3过量时显然发生反应8NH3+3Br2=N2+6NH4Br。
,当NH3过量时显然发生反应8NH3+3Br2=N2+6NH4Br。
(3)要在A中充满与大气压相等的HCl气体,需在A与大气联通的条件下充入,因P(HCl)>P空气,故需打开K1,在K2处通入至K1处有HCl逸出(有白雾出现);若缓慢打开K3,则会因NH3进入A管并发生反应NH3+HCl====NH4Cl而产生白烟,压强减小,石蜡油充满B管(剩余的NH3恰好充满A管),若观察不到上述现象,则可能由于HCl中混有空气或石蜡两端的液面不平,内部气体压强不等于大气压所造成。
答案:(1)

(2)8NH3+3Br2====N2+6NH4Br(或2NH3+3Br2====N2+6HBr)
(3)①先开K1,再开K2,从K2处通入干燥的HCl气体,管口K1处有白雾后继续通入一段时间,关闭K2,随即关闭K1。②产生白烟 石蜡油充满B管
A管中未全部充满干燥HCl气体,混有空气,未使石蜡油两端液面相平

 阅读快车系列答案
阅读快车系列答案化学反应速率与化学平衡在日常生活、工农业生产和科学研究中具有重要的意义,在
化学实验中涉及的电离平衡也属于化学平衡。请回答下列问题:
(1)某研究性学习小组查阅资料发现金属氧化物A也能催化氯酸钾的分解,且A和二
氧化锰的最佳催化温度均为500℃左右。于是对A和二氧化锰的催化性能进行了
定量对照实验。实验时均以收满500 mL氧气为准(其他可能影响实验的因素均已
忽略)。
表一 用MnO2作催化剂
| 实验序号 | KClO3质量/g | MnO2质量/g | 反应温度/℃ | 待测数据 |
| 1 | 8.00 | 2.00 | 500 | |
| 2 | 8.00 | 2.00 | 500 |
表二 用A作催化剂
| 实验序号 | KClO3质量/g | A的质量/g | 反应温度/℃ | 待测数据 |
| 1 | 8.00 | 2.00 | 500 | |
| 2 | 8.00 | 2.00 | 500 |
请回答:上述实验中的待测数据应是 。
完成此研究后,他们准备发表一篇研究报告,请你替他们拟一研究报告的标题:
。
(2)氨水是一种弱碱,某同学取0.1mo/L的氨水,用pH试纸测其pH,结果发现溶液的
pH约为11,以此得出氨水为弱碱的结论。该同学用pH试纸测定氨水pH的具体操
作是 。
(3)证明氨水是弱碱的常用方法还有两种:一是设法证明NH![]() 的水解,一是设法使氨水
的水解,一是设法使氨水
电离平衡发生移动。
方法一:取少量NH4Cl晶体溶于水,滴入石蕊试液,溶液变红,可见溶液显酸性。
其原因是 。
方法二:取少量氨水,滴入酚酞变红后再加入 ,振荡,红色变浅,c(OH—)下降,说明氨水的电离平衡向 移动。