题目内容
12.有下列六种转化途径,某些反应条件和产物已省略,下列有关说法正确的是( )途径①Fe$\stackrel{稀HCl}{→}$FeCl2溶液 途径②Fe$\stackrel{Cl_{2}}{→}$FeCl3$\stackrel{Fe、水}{→}$FeCl2溶液
途径③Cl2$\stackrel{Na_{2}SO_{3}溶液}{→}$Na2SO4溶液 途径④Cl2$\stackrel{NaOH溶液}{→}$NaCIO溶液$\stackrel{Na_{2}SO_{3}溶液}{→}$Na2SO4溶液
途径⑤S$\stackrel{弄HNO_{3}}{→}$ H2SO4 途径⑥S$\stackrel{O_{2}}{→}$SO2$\stackrel{O_{2}}{→}$SO3$\stackrel{H_{2}O}{→}$H2SO4.
| A. | 由途径①和②分别制取1molFeCl2,理论上各消耗1molFe,各转移2mole- | |
| B. | 由途径③和④分别制取1 mol Na2SO4,理论上各消耗1 molCl2,各转移2mole- | |
| C. | 由途径⑤和⑥分别制取1 mol H2SO4,理论上各消耗1molS,各转移6mole- | |
| D. | 以上说法都不正确 |
分析 A.途径①,Fe元素化合价由0升高为+2,途径②Fe元素化合价由0升高为+3,然后发生2FeCl3+Fe=3FeCl2;
B.途径③制取1 mol Na2SO4,转移2mol电子,而④发生两步氧化还原反应,NaClO溶液$\stackrel{Na_{2}SO_{3}溶液}{→}$1molNa2SO4中转移2mol电子;
C.途径⑤和⑥分别制取1 mol H2SO4,S元素的化合价均由0升高为+6价;
D.由上述分析判断.
解答 解:A.途径①,Fe元素化合价由0升高为+2,制取1molFeCl2,理论上消耗1molFe,转移2mole-,而途径②Fe元素化合价由0升高为+3,然后发生2FeCl3+Fe=3FeCl2,总反应中Fe失去电子变化为亚铁离子,理论上制取1molFeCl2,理论上消耗1molFe,转移2mole-,故A正确;
B.途径③制取1 mol Na2SO4,转移2mol电子,而④发生两步氧化还原反应,NaClO溶液$\stackrel{Na_{2}SO_{3}溶液}{→}$1molNa2SO4中转移2mol电子,则④转移电子多,故B错误;
C.途径⑤和⑥分别制取1 mol H2SO4,S元素的化合价均由0升高为+6价,则理论上各消耗1mol S,各转移6mol e-,故C正确;
D.由上述分析可知,A、C合理,故D错误;
故选AC.
点评 本题考查物质的性质及氧化还原反应,把握发生的反应中元素的化合价变化为解答的关键,注意理论计算中化合价与转移电子的关系,题目难度中等.

练习册系列答案
相关题目
2.常温下,下列溶液中各微粒浓度关系正确的是( )
| A. | pH相等的①CH3COONa ②C6H5ONa ③NaHCO3溶液中,c(Na+)大小关系:①>②>③ | |
| B. | 向氨水中滴加稀硫酸至溶液呈中性:c(NH4+)>c(SO42-)>c(OH-)=c(H+) | |
| C. | 向1L0.1mol/L的NaOH溶液中通入6.6gCO2:2c(Na+)=3[c(CO32-)+c(HCO${\;}_{3}^{-}$)+c(H2CO3)] | |
| D. | CH3COONa溶液中加入少量KNO3后的碱性溶液一定有:c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
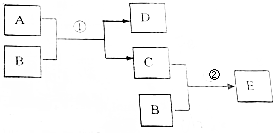
20.一定条件下,甲组内任意一种物质和乙组内任意一种物质都能发生反应的是
( )
| 甲 | 乙 | |
| A | H2、O2 | N2、CuO |
| B | HCl、NaOH | Fe、Al |
| C | SiO2、浓H2SO4 | NaOH、C |
| D | CO2、H2O | Na2O2、NaCl |
| A. | A | B. | B | C. | C | D. | D |
7.8.34g FeSO4•7H2O(分子量:278)样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示,下列说法正确的是( )

| A. | 温度为78℃时固体物质M的化学式为FeSO4•5H2O | |
| B. | 取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,Q的化学式为Fe3O4 | |
| C. | 在隔绝空气条件下,N得到P的化学方程式为FeSO4•H2O $\frac{\underline{\;高温\;}}{\;}$FeSO4+H2O | |
| D. | 温度为l59℃时固体N的化学式为FeSO4•2H2O |
17.能正确表示下列反应的离子方程式是( )
| A. | 用铜做电极电解CuSO4溶液:2Cu2++2H2O═2Cu+O2↑+4H+ | |
| B. | NaClO溶液与FeCl2溶液混合:Fe2++2ClO-+2H2O═Fe(OH)2↓+2HClO | |
| C. | NH4HSO3溶液与足量NaOH溶液共热:NH${\;}_{4}^{+}$+H++2OH-═NH3↑+2H2O | |
| D. | 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+ |
4.NA 表示阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 1mol 12C原子的质量是12g,1个12C原子的质量是$\frac{12}{{N}_{A}}$g | |
| B. | 在常温常压下,11.2LN2含有分子数为0.5NA | |
| C. | 18g水所含有的氢原子数目为2NA,氧原子数目为NA | |
| D. | 1L 0.1mol•L-1K2SO4溶液中,K+ 和SO42-的离子总数是0.3NA |
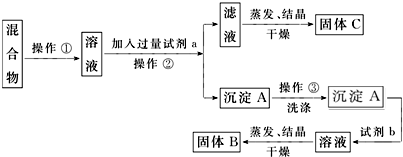
16.某化学兴趣小组设计如下流程,从酸性工业废液(含H+、Al3+、Mg2+、Cr3+、SO${\;}_{4}^{2-}$)中提取铬.

有关数据如表:
回答下列问题:
(1)步骤①所得滤液可用于制取MgSO4•7H2O,酸性工业废液中加入适量氧化铝的作用是调节溶液的pH.
(2)若酸性废液中c(Mg2+)=0.lmol.L-l,为达到步骤①的实验目的,则废液的pH应保持在(5.3,7.8)范围(保留小数点后l位).
(3)步骤②中生成NaCrO2的离子方程式为Cr(OH)3+OH-=CrO2-+2H2O.
(4)步骤④中反应的离子方程式为7H2O+4CrO42-+6S=4Cr(OH)3↓+3S2O32-+2OH-.
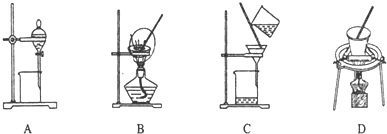
(5)步骤⑤在空气中充分灼烧的目的是使Cr(OH)3完全转化为Cr2O3,可选用的装置是D(填序号).
(6)用如图所示装置制取铬酸钠(Na2CrO4),回答相关问题.
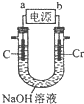
①a是电源的负极,阳极的电极反应式为Cr-6e-+8OH-=CrO42-+4H2O.
②若电解一段时间后阴极收集到标准状况下的气体3.36L,则理论上可制得8.1g铬酸钠(忽略反应2CrO42-(aq)+2H+(aq)?Cr2O72-(aq)+H2O(1)的影响)

有关数据如表:
| 化合物 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
| 完全沉淀的Ph | 10.5 | 4.3 | 5.3 |
| 开始溶解的pH | -- | 7.8 | 9.2 |
| Ksp近似值 | 10-12 | 10-14 | 10-31 |
(1)步骤①所得滤液可用于制取MgSO4•7H2O,酸性工业废液中加入适量氧化铝的作用是调节溶液的pH.
(2)若酸性废液中c(Mg2+)=0.lmol.L-l,为达到步骤①的实验目的,则废液的pH应保持在(5.3,7.8)范围(保留小数点后l位).
(3)步骤②中生成NaCrO2的离子方程式为Cr(OH)3+OH-=CrO2-+2H2O.
(4)步骤④中反应的离子方程式为7H2O+4CrO42-+6S=4Cr(OH)3↓+3S2O32-+2OH-.
(5)步骤⑤在空气中充分灼烧的目的是使Cr(OH)3完全转化为Cr2O3,可选用的装置是D(填序号).

(6)用如图所示装置制取铬酸钠(Na2CrO4),回答相关问题.

①a是电源的负极,阳极的电极反应式为Cr-6e-+8OH-=CrO42-+4H2O.
②若电解一段时间后阴极收集到标准状况下的气体3.36L,则理论上可制得8.1g铬酸钠(忽略反应2CrO42-(aq)+2H+(aq)?Cr2O72-(aq)+H2O(1)的影响)