题目内容
19.一定温度下,在一个固定容积的密闭容器中加入3molH2和1molN2,建立如下平衡:N2(g)+3H2(g)?2NH3(g)相同条件下,若向容器中再通入3mol H2和,1molN2再次达到平衡.则下列说法正确的是( )
| A. | NH3的百分含量不变 | B. | N2的体积分数增大 | ||
| C. | N2的转化率增大 | D. | NH3的百分含量增小 |
分析 假设恒温、恒压则互为等效平衡,转化率和百分含量保持不变.而恒温、恒压当物质的量增大时体积必然增大,故恒温、恒容必然在等效的基础上加压使平衡向右移动.
解答 解:一定温度下,在一个固定容积的密闭容器中加入3molH2和1molN2,建立如下平衡:N2(g)+3H2(g)?2NH3(g)相同条件下,若向容器中再通入3mol H2和,1molN2再次达到平衡,假设恒温、恒压则互为等效平衡,转化率和百分含量保持不变.而恒温、恒压当物质的量增大时体积必然增大,故恒温、恒容必然在等效的基础上加压,反应是气体体积减小的反应,增大压强使平衡向右移动,
A、平衡正向进行氨气百分含量增大,故A错误;
B、平衡正向进行N2的体积分数减小,故B错误;
C、平衡正向进行N2的转化率增大,故C正确;
D、平衡正向进行NH3的百分含量增大,故D错误;
故选C.
点评 本题考查了化学平衡的影响因素分析判断,主要是反应特征,平衡移动原理的理解应用,掌握基础是解题关键,题目较简单.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
10.下列化学用语正确的是( )
| A. | 次氯酸钙的化学式:CaClO | |
| B. | 氟离子结构示意图: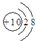 | |
| C. | 质量数为137的钡原子:${\;}_{137}^{56}$Ba | |
| D. | 硫酸的电离方程式:H2SO4=2H++SO42- |
4.有机物分子中基团之间的相互影响会导致物质化学性质的不同.下列事实能说明上述观点的是 ( )
| A. | 苯酚能跟NaOH溶液反应,乙醇不能与NaOH溶液反应 | |
| B. | 乙烯能发生加成反应,乙烷不能发生加成反应 | |
| C. | 甲苯能使酸性高锰酸钾溶液褪色,苯不能使酸性高锰酸钾溶液褪色 | |
| D. | 苯在50℃~60℃时发生硝化反应,而甲苯在30℃时即可 |
11.下列说法正确的是( )
| A. | 按系统命名法: 的名称为3,3,6三甲基4乙基庚烷 的名称为3,3,6三甲基4乙基庚烷 | |
| B. | 如图是某有机物分子的比例模型,该物质可能是一种氨基酸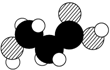 | |
| C. | 能用新制氢氧化铜和NaOH溶液鉴别甘油、葡萄糖溶液、乙酸钠溶液 | |
| D. | 木糖醇( 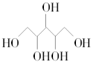 )和葡萄糖( )和葡萄糖(  )互为同系物,均属于糖类 )互为同系物,均属于糖类 |
9.下列不能达到实验目的是( )
| A. | 将等物质的量的CH4和Cl2在光照下反应生成纯净的CH3Cl | |
| B. | 将苯与浓硝酸和浓硫酸混合水浴加热制取硝基苯 | |
| C. | 用新制Cu(OH)2悬浊液鉴别葡萄糖和蔗糖 | |
| D. | 用浓硝酸鉴别淀粉溶液和鸡蛋白溶液 |
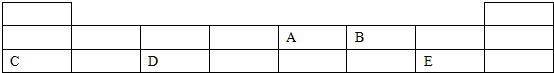
 ;B元素在周期表中的位置是第二周期ⅥA族.A比B的非金属性弱(填“强”或“弱”).
;B元素在周期表中的位置是第二周期ⅥA族.A比B的非金属性弱(填“强”或“弱”). ,而不排布成
,而不排布成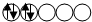 ,其直接的根据是洪特规则.
,其直接的根据是洪特规则.