题目内容
某化工厂的含镍废催化剂主要含Ni,还含有Al、Al2O3、Fe、FeO、Fe2O3及其他不溶杂质(其他不溶杂质不与酸碱反应)。某校化学研究性学习小组设计了如下图所示的方法,以该含镍废催化剂为原料来制备NiSO4·7H2O。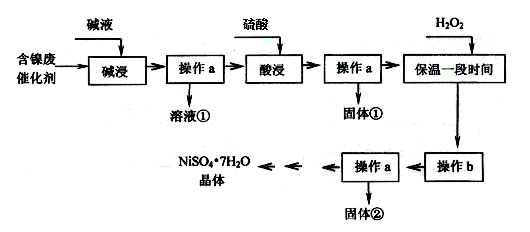
【查阅资料】
①Ni能与非氧化性酸反应生成Ni2+,不与碱液反应。
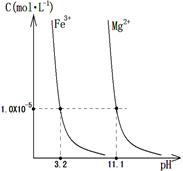
②部分阳离子以氢氧化物形式沉淀时pH如下:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀的pH | 4.1 | 1.7 | 7.6 | 7.0 |
| 完全沉淀的pH | 5.2 | 3.2 | 9.5 | 9.2 |
(1)操作a为 。
(2)“碱浸”的目的是除去 (填化学式)。
(3)操作b为调节溶液的pH,你认为pH的最佳调控范围是 。
(4)NiSO4在强碱溶液中用次氯酸钠氧化,可以制得碱性镍氢电池电极材料NiOOH。
①写出该反应的离子方程式 。
②已知碱性镍氢电池总反应: H2+2NiOOH
 2Ni(OH)2,写出该反应放电时正极反应式 。
2Ni(OH)2,写出该反应放电时正极反应式 。(5)一般认为残留在溶液中的离子浓度小于1.0×10-5 mol·L-1时,沉淀已经完全。请利用上表中数据估算Fe(OH)2的溶度积
 。
。
(1)过滤 (2分) (2)Al、Al2O3(2分) (3)3.2≤pH<7.0 (2分)
(4)①2Ni2++ClO-+4OH-=2NiOOH+Cl-+H2O(3分) ②NiOOH + H2O + e- = Ni(OH)2 + OH- (3分)
(5)1.0×10-14 mol3·L-3(2分)
解析试题分析:(1)捏Ni、Fe、FeO、Fe2O3及其他不溶杂质均不与碱反应,所以碱液浸后金属铝、氧化铝溶解,其它物质不溶,过滤即可除去,所以操作a是过滤。
(2)“碱浸”的目的是除去含镍废催化剂Al、Al2O3。
(3)由于前面加入了氧化剂双氧水,所以溶液中的亚铁离子被氧化生成了铁离子。根据表中数据可知,铁离子完全沉淀时的pH值是3.2,而Ni2+开始沉淀时的pH值是7.0,因此操作b应该控制溶液的pH值为3.2≤pH<7.0。
(4)①NiSO4在强碱溶液中用次氯酸钠氧化,可以制得碱性镍氢电池电极材料NiOOH,在反应中氯元素的化合价从+1价降低到-1价,得到2个电子。而Ni元素的化合价从+2价升高到+3价失去1个电子,所以还原剂硫酸镍与氧化剂次氯酸钠的物质的量之比是2:1,因此反应的离子方程式为2Ni2++ClO-+4OH-=2NiOOH+Cl-+H2O。
②原电池中负极失去电子,发生氧化反应。电子经导线传递到正极,所以正极得到电子,发生还原反应。根据方程式可知放电时氢气是还原剂失去电子,NiOOH是氧化剂得到电子,做正极,因此正极电极反应式为NiOOH + H2O + e- = Ni(OH)2 + OH-。
③根据表中数据可知,氢氧化亚铁完全沉淀时的pH值是9.5,根据氢氧化亚铁的溶度积常数表达式Ksp=c(Fe2+)·c2(OH-),氢氧化亚铁的溶度积常数Ksp=1.0×10-5 mol·L-1×(10-4.5mol/L)2=1.0×10-14 mol3·L-3。
考点:考查物质制备工艺流程的有关判断、溶度积常数的有关计算与应用、氧化还原反应方程式的书写以及电极反应式的书写等

 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案现有A、B、C、D、E五种可溶强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
| 阳离子 | H+、Na+、Al3+、Ag+、Ba2+ |
| 阴离子 | OH-、Cl-、CO32-、NO3-、SO42- |
已知:①A、B两溶液呈碱性; C、D、E溶液呈酸性。
②向E溶液中逐滴滴加B溶液至过量,沉淀量先增加后减少但不消失。
③D溶液与另外四种溶液反应都能产生沉淀。
试回答下列问题:
(1)A溶液呈碱性的原因是 (用离子方程式表示)。
(2)写出E溶液与过量的B溶液反应的离子方程式 。
(3)若25°时C、E溶液pH=4,则E溶液中水电离出的氢离子浓度是C溶液中水电离出的氢离子
浓度 倍。
(4)将C溶液逐滴加入等体积、等物质的量的浓度的A溶液中,反应后溶液中一价离子(+1或-1)
浓度由大到小的顺序为: 。
已知:在室温时H2O H++OH- KW=10-14 CH3COOH
H++OH- KW=10-14 CH3COOH  H++ CH3COO- Ka=1.8×10-5
H++ CH3COO- Ka=1.8×10-5
(1)取适量醋酸溶液,加入少量醋酸钠固体,此时溶液中C(H+)与C(CH3COOH)的比值 (填“增大”或“减小”或“不变”)
(2)醋酸钠水解的离子方程式为 。当升高温度时,C(OH—)将 (填“增大”“减小”“不变”);
(3)0.5mol·L-1醋酸钠溶液pH为m,其水解的程度(已水解的醋酸钠与原有醋酸钠的比值)为a;1mol·L-1醋酸钠溶液pH为n,水解的程度为b,则m与n的关系为 ,a与b的关系为 (填“大于”“小于”“等于”);
(4)将等体积等浓度的醋酸和氢氧化钠溶液混合后,所得溶液中离子浓度由大到小的顺序是 。
(5)若醋酸和氢氧化钠溶液混合后pH<7,则c(Na+)_______________ c(CH3COO-)(填“大于”、“小于”或“等于”),
(6)室温时,若由pH=3的HA溶液V1mL与pH=11的NaOH溶液V2 mL混合,则下列说法不正确的是____________。
| A.若反应后溶液呈中性,则c(H+)+c(OH-)=2×10-7mol·L-1 |
| B.若V1=V2,反应后溶液pH一定等于7 |
| C.若反应后溶液呈酸性,则V1一定大于V2 |
| D.若反应后溶液呈碱性,则V1一定小于V2 |
体醋酸钠后测得溶液的C(OH-)为2.2×10-5mol·L-1,以上三种金属离子中 能生成沉淀,原因是 。
(KSP[Mg(OH)2]=1.8×10-11、KSP[Zn(OH)2]=1.2×10-17、
KSP[Cd(OH)2]=2.5×10-14)
(8)取10mL0.5mol·L-1盐酸溶液,加水稀释到500mL,则该溶液中由水电离出的c(H+)
= mol/L。
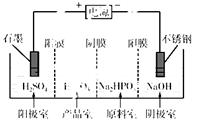
 H+ + H2PO3-。亚磷酸与足量NaOH溶液反应,生成Na2HPO3。
H+ + H2PO3-。亚磷酸与足量NaOH溶液反应,生成Na2HPO3。