题目内容
【题目】二氯化二硫(S2Cl2)在工业上用于橡胶的硫化,还可以作为贵金属的萃取剂。可由硫和氯气在100~110℃直接化合而成。实验室用以下装置制备S2Cl2并对尾气进行回收利用。已知S2Cl2的熔点:-77℃,沸点:137℃。S2Cl2遇水剧烈反应。
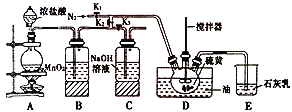
(1)反应前必须进行的操作是:__________。
(2)写出装置A中发生反应的离子方程式:__________。
(3)B中所装试剂名称为__________, 其作用是__________。
(4)通入N2的目的是__________。
A、B装置中的空气可以通过控制K2、K3来去除,具体方法为__________。
(5)S2Cl2遇水会生成淡黄色单质、一种能使品红溶液褪色的气体化合物和酸雾,写出该反应的化学方程式__________。
(6)实验时,D装置开始需要油浴加热一段时间,之后停止加热,仅需通入氯气即可。则生成二氯化二硫的反应为__________(填“放热”或“吸热”)反应。
(7)该装置由于存在缺陷,使制得的二氯化二硫可能不纯,简述改进方法__________。
【答案】 检查装置气密性 MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O 浓硫酸 干燥氯气 排尽装置中的空气,防止硫加热时与氧气反应 关闭K2打开K3,当B装置上方充满黄绿色气休时,关闭K3打开K2 2S2Cl2+2H2O=SO2↑+3S↓+4HCl 放热 在D与E之间增加1个装有无水氯化钙(或五氧化二磷或硅胶)的干燥管或装有浓硫酸的洗气瓶
Mn2++Cl2↑+2H2O 浓硫酸 干燥氯气 排尽装置中的空气,防止硫加热时与氧气反应 关闭K2打开K3,当B装置上方充满黄绿色气休时,关闭K3打开K2 2S2Cl2+2H2O=SO2↑+3S↓+4HCl 放热 在D与E之间增加1个装有无水氯化钙(或五氧化二磷或硅胶)的干燥管或装有浓硫酸的洗气瓶
【解析】(1)反应过程中有氯气参与,反应前必须检查装置气密性,故答案为:检查装置气密性;
(2)装置A中二氧化锰与浓盐酸反应生成氯气,反应的离子方程式为MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(3)制得的氯气中混有氯化氢和水蒸气,因为S2Cl2遇水剧烈反应,因此反应前需要干燥氯气,B中装入浓硫酸即可,故答案为:浓硫酸;干燥氯气;
(4)反应需要在100~110℃下进行,为了防止硫加热时与氧气反应,需要通入N2,排尽装置中的空气,A、B装置中的空气可以通过控制K2、K3来去除,具体方法为关闭K2打开K3,当B装置上方充满黄绿色气休时,关闭K3打开K2,故答案为:排尽装置中的空气,防止硫加热时与氧气反应;关闭K2打开K3,当B装置上方充满黄绿色气休时,关闭K3打开K2;
(5) S2Cl2遇水会生成淡黄色单质为S、一种能使品红溶液褪色的气体化合物为二氧化硫和酸雾为氯化氢,反应的化学方程式为,故答案为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl;
(6)实验时,D装置开始需要油浴加热一段时间,之后停止加热,仅需通入氯气即可,说明生成二氯化二硫的反应为放热反应,故答案为:放热;
(7) S2Cl2遇水剧烈反应,反应装置中,E中的水蒸气可以通过导管进入D中,使制得的二氯化二硫不纯,改进方法为在D与E之间增加1个装有无水氯化钙(或五氧化二磷或硅胶)的干燥管或装有浓硫酸的洗气瓶,故答案为:在D与E之间增加1个装有无水氯化钙(或五氧化二磷或硅胶)的干燥管或装有浓硫酸的洗气瓶。