题目内容
某校化学小组学生进行“气体相对分子质量的测定”的实验。操作如下:用质量和容积都相等的烧瓶收集气体,称量收集满气体的烧瓶质量,数据见下表(已换算成标准状况下的数值)。
已知标准状况下,烧瓶的容积为0.293 L,烧瓶和空气的总质量为48.4212 g,空气的平均相对分子质量为29。A、B、C、D、E是中学常见的气体。
(1)上述五种气体中,能够使品红溶液褪色的是(写化学式)________.
(2)D的相对分子质量是________。
(3)在标准状况下,11.2 L D气体中含有共用电子对的数目为________。
(4)A、B、C可能的化学式是________。
| 气体 | 烧瓶和气体的总质量(g) |
| A | 48.4082 |
| B | 48.4082 |
| C | 48.4082 |
| D | 48.4342 |
| E | 48.8762 |
已知标准状况下,烧瓶的容积为0.293 L,烧瓶和空气的总质量为48.4212 g,空气的平均相对分子质量为29。A、B、C、D、E是中学常见的气体。
(1)上述五种气体中,能够使品红溶液褪色的是(写化学式)________.
(2)D的相对分子质量是________。
(3)在标准状况下,11.2 L D气体中含有共用电子对的数目为________。
(4)A、B、C可能的化学式是________。
(1)SO2 (2)30 (3)3.5NA或2.107×1024 (4)N2、CO、C2H4
设烧瓶的质量为m,盛空气时,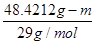 =
=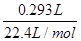 ,m=48.04 g,据阿伏加德罗定律可得:
,m=48.04 g,据阿伏加德罗定律可得:
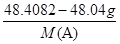 =
=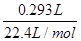 ,
,
解得M(A)≈28 g/mol=M(B)=M(C),所以A、B、C可能为N2、CO、C2H4,同理可推出D、E的相对分子质量分别约为30、64,所以D为C2H6,E为SO2(能使品红溶液褪色)。
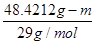 =
=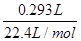 ,m=48.04 g,据阿伏加德罗定律可得:
,m=48.04 g,据阿伏加德罗定律可得: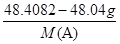 =
=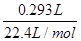 ,
,解得M(A)≈28 g/mol=M(B)=M(C),所以A、B、C可能为N2、CO、C2H4,同理可推出D、E的相对分子质量分别约为30、64,所以D为C2H6,E为SO2(能使品红溶液褪色)。

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
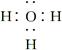
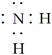
 S2-+H3O+
S2-+H3O+