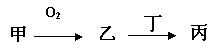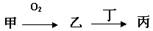题目内容
已知:在常温常压下,A、B、C、D、E、F、G都是气体,其中A、G有颜色,C是相对分子质量最小的气体,B、F是空气的主要成分.各物质间转化关系如图:试回答下列问题:

(1)在①、②反应中MnO2的作用分别为 ①
(2)F的结构式为
(4)写出③的化学反应方程式

(1)在①、②反应中MnO2的作用分别为 ①
氧化剂
氧化剂
、②催化剂
催化剂
.(2)F的结构式为
N≡N
N≡N
.(3)E、D相遇时观察到的现象是冒白烟
冒白烟
.(4)写出③的化学反应方程式
3Cl2+2NH3=N2+6HCl
3Cl2+2NH3=N2+6HCl
.无色液体乙与SO2反应的离子方程式为H2O2+SO2=2H++SO42-
H2O2+SO2=2H++SO42-
.分析:在常温常压下,A、B、C、D、E、F、G都是气体,C是相对分子质量最小的气体,为H2,B、F是空气的主要成分,为N2和O2,A、G有颜色,为Cl2和NO2;
由反应①MnO2+无色溶液甲→A,故A为Cl2,甲为盐酸,结合上述可知G为NO2,由反应②MnO2+无色溶液乙→B,故B为O2,乙为H2O2,结合上述可知F为N2;
由反应③A+C→E可知,E为HCl,由A+D→E+F,根据元素守恒可知,D含有N、H两种元素,故D为NH3.
由反应①MnO2+无色溶液甲→A,故A为Cl2,甲为盐酸,结合上述可知G为NO2,由反应②MnO2+无色溶液乙→B,故B为O2,乙为H2O2,结合上述可知F为N2;
由反应③A+C→E可知,E为HCl,由A+D→E+F,根据元素守恒可知,D含有N、H两种元素,故D为NH3.
解答:解:在常温常压下,A、B、C、D、E、F、G都是气体,C是相对分子质量最小的气体,为H2,B、F是空气的主要成分,为N2和O2,A、G有颜色,为Cl2和NO2;
由反应①MnO2+无色溶液甲→A,故A为Cl2,甲为盐酸,结合上述可知G为NO2,由反应②MnO2+无色溶液乙→B,故B为O2,乙为H2O2,结合上述可知F为N2;
由反应③A+C→E可知,E为HCl,由A+D→E+F,根据元素守恒可知,D含有N、H两种元素,故D为NH3,
(1)反应①为MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,反应中Mn元素的化合价降低,MnO2是氧化剂;
反应②为2H2O2
2H2O+O2↑,MnO2的作用是催化剂,故答案为:氧化剂;催化剂;
(2)F为N2,分子中氮原子之间形成3对共用电子对,结构式为:N≡N,故答案为:N≡N;
(3)氯化氢与氨气反应生成氯化铵,故二者相遇时现象是:冒白烟,故答案为:冒白烟;
(4)反应③是氯气与氨气反应生成氮气与氯化氢,反应方程式为:3Cl2+2NH3=N2+6HCl;
H2O2有强氧化性,与SO2反应生成硫酸,反应离子方程式为:H2O2+SO2=2H++SO42-,
故答案为:3Cl2+2NH3=N2+6HCl;H2O2+SO2=2H++SO42-.
由反应①MnO2+无色溶液甲→A,故A为Cl2,甲为盐酸,结合上述可知G为NO2,由反应②MnO2+无色溶液乙→B,故B为O2,乙为H2O2,结合上述可知F为N2;
由反应③A+C→E可知,E为HCl,由A+D→E+F,根据元素守恒可知,D含有N、H两种元素,故D为NH3,
(1)反应①为MnO2+4HCl(浓)
| ||
反应②为2H2O2
| ||
(2)F为N2,分子中氮原子之间形成3对共用电子对,结构式为:N≡N,故答案为:N≡N;
(3)氯化氢与氨气反应生成氯化铵,故二者相遇时现象是:冒白烟,故答案为:冒白烟;
(4)反应③是氯气与氨气反应生成氮气与氯化氢,反应方程式为:3Cl2+2NH3=N2+6HCl;
H2O2有强氧化性,与SO2反应生成硫酸,反应离子方程式为:H2O2+SO2=2H++SO42-,
故答案为:3Cl2+2NH3=N2+6HCl;H2O2+SO2=2H++SO42-.
点评:本题以无机框图题的形式考查N、O、Cl等元素单质及其化合物之间的相互转化关系和逻辑推理能力、化学用语的书写、氧化还原反应等,难度中等,题中A、G有颜色,C是相对分子质量最小的气体,B、F是空气的主要成分为解题突破口,结合转化关系推断,反应③是陌生的知识,利用倒推法确定,对学生的逻辑推理能力提出较高要求.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
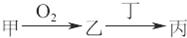 甲、乙、丙三种物质都含有A元素,只有甲是单质,其转化关系如图所示:
甲、乙、丙三种物质都含有A元素,只有甲是单质,其转化关系如图所示: