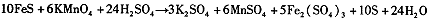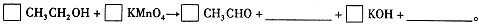题目内容
铋(Bi)位于元素周期表中VA族,其价态为+3时较稳定,铋酸钠(NaBiO3)可氧化硫酸锰(MnSO4),反应的离子方程式为5NaBiO3+2Mn2++14H+=2MnO- 4+5Bi3++Na++7H2O,下列说法错误的是
| A.若有0.1mol氧化产物生成,则转移0.5mol电子 |
| B.铋酸钠难溶于水 |
| C.该反应可以用于鉴定Mn2+离子 |
| D.该反应可以用浓盐酸酸化 |
D
试题分析:A、反应中转移电子为10个,若有0.1mol氧化产物(MnO- 4)生成,则转移0.5mol电子,正确;B、离子方程式为5NaBiO3+2Mn2++14H+=2MnO- 4+5Bi3++Na++7H2O,NaBiO3未拆成离子说明铋酸钠难溶于水,正确;C、若有Mn2+离子,反应后溶液出现紫色,正确;D、Cl-的还原性强于Mn2+离子,会先与NaBiO3反应,错误。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 HNO3。写出OH与NO反应的化学方程式:_____________,该反应中被氧化的元素是 。
HNO3。写出OH与NO反应的化学方程式:_____________,该反应中被氧化的元素是 。


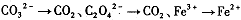 ,找出其中一个变化与“
,找出其中一个变化与“ ”组成一个反应,写出该反应的离子方程式____ 。
”组成一个反应,写出该反应的离子方程式____ 。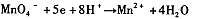
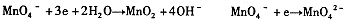 由此可知,高锰酸根离子(MnO—4)反应后的产物与 有关。
由此可知,高锰酸根离子(MnO—4)反应后的产物与 有关。