题目内容
【题目】(1)一个体重50 kg的健康人含铁元素2 g,这2 g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4)。服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收。
①人体中经常进行Fe2+与Fe3+的转化,可表示为Fe2+![]() Fe3+。“服用维生素C可使食物中的Fe3+转化为Fe2+”, 由此可以推知维生素C在该过程中作__________剂。
Fe3+。“服用维生素C可使食物中的Fe3+转化为Fe2+”, 由此可以推知维生素C在该过程中作__________剂。
②腌制食品中含有亚硝酸盐,亚硝酸盐能使人体内的铁元素发生A过程,过多食用会发生食物中毒,Fe2+此过程中表现出________性。
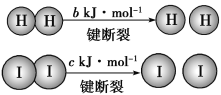
③已知下列反应在一定条件下发生:
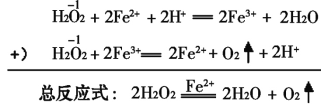
在以上的反应中,Fe2+实际上起着 ______________的作用。
(2)硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
①下列物质不是硅酸盐材料的是(________)
A.陶瓷 B.玻璃 C.水泥 D.生石灰
②SiO2是玻璃的成分之一,SiO2与氢氧化钠溶液反应的离子方程式________,工艺师常用________(填物质名称)来雕刻玻璃。
③试管中加入3~5mL Na2SiO3溶液,滴入1~2滴酚酞溶液,再用胶头滴管逐滴加入稀盐酸,边加边振荡,至溶液红色变浅接近消失时停止,静置即得到硅酸胶体,该反应的化学方程式为__________________________________。
【答案】还原 还原 催化剂 D SiO2 + 2OH─ = SiO![]() + H2O 氢氟酸 Na2SiO3 + 2HCl = H2SiO3(胶体) + 2 NaCl
+ H2O 氢氟酸 Na2SiO3 + 2HCl = H2SiO3(胶体) + 2 NaCl
【解析】
(1)①![]() 转化为
转化为![]() ,得电子被还原,因此维生素C作还原剂;
,得电子被还原,因此维生素C作还原剂;
②![]() 转变为
转变为![]() ,失电子被氧化,则
,失电子被氧化,则![]() 在该过程中作还原剂;
在该过程中作还原剂;
③![]() 在反应中先消耗后生成,反应前后数量不变,因此起到催化剂的作用;
在反应中先消耗后生成,反应前后数量不变,因此起到催化剂的作用;
(2)①玻璃、陶瓷、水泥为三大硅酸盐材料,生石灰是![]() ,不属于硅酸盐,答案选D;
,不属于硅酸盐,答案选D;
②![]() 作为酸性氧化物可以与碱反应得到盐和水:
作为酸性氧化物可以与碱反应得到盐和水:![]() ,在蚀刻玻璃时经常使用氢氟酸来进行;
,在蚀刻玻璃时经常使用氢氟酸来进行;
③硅酸是一种弱酸,可以由强酸和硅酸盐反应制得:![]() 。
。