题目内容
加热16.8gNaHCO3至没有气体放出时,剩余的物质是什么?计算剩余物质的质量和物质的量。
(1)加热NaHCO3时发生的化学反应:___________________________
(2)剩余的物质是 ,质量为 ,物质的量为 。(写出计算过程)
【答案】
(1)加热NaHCO3时发生的化学反应为:2NaHCO3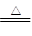 Na2CO3+H2O+CO2↑(2分)
Na2CO3+H2O+CO2↑(2分)
(2)剩余物质是Na2CO3,10.6g,0.1mol(4分)
【解析】
试题分析:碳酸氢钠加热分解成碳酸钠、水和二氧化碳。
2NaHCO3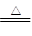 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
168 106
16.8g m(Na2CO3)
106m(Na2CO3)= 16.8g*106
解得:m(Na2CO3)=10.6g
N(Na2CO3)=10.6g/106(g/mol)=0.1mol
考点:无机反应
点评:本题考查了碳酸氢钠的性质,题目不难解答,考查内容源自于教材,另考查了学生的计算能力。

练习册系列答案
相关题目