题目内容
【题目】用“银-Ferrozine”法测室内甲醛含量的原理为:
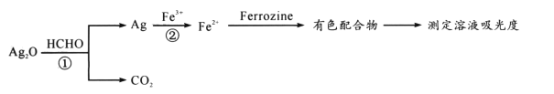
已知:吸光度与溶液中有色物质的浓度成正比
下列说法正确的是
A. 反应①中参与反应的HCHO为30g时转移电子2mol
B. 可用双氧水检验反应②后的溶液中是否存在Fe3+
C. 生成44.8 LCO2时反应②中参加反应的Ag一定为8mol
D. 理论上测得溶液吸光度越高,HCHO含量也越高
【答案】D
【解析】
A. 30g HCHO的物质的量为1mol,被氧化时生成二氧化碳,碳元素化合价从0价升高到+4价,所以转移电子4mol,故A错误;
B.过氧化氢能将Fe2+氧化为Fe3+,与Fe3+不反应,所以不能用双氧水检验反应②后的溶液中是否存在Fe3+,故B错误;
C. 没有注明温度和压强,所以无法计算气体的物质的量,也无法计算参加反应的Ag的物质的量,故C错误;
D. 吸光度与溶液中有色物质的浓度成正比,吸光度越高,则说明反应②生成的Fe2+越多,进一步说明反应①生成的Ag越多,所以HCHO含量也越高,故D正确。
故选D。

练习册系列答案
相关题目